
【題目】大運會時深圳新能源汽車上有一種質子交換膜燃料電池,工作原理如圖所示,下列敘述正確的是( )
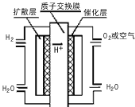
A.通入氧氣的電極發生氧化反應
B.通入氫氣的電極為正極
C.總反應式為O2+2H2![]() 2H2O
2H2O
D.正極的電極反應式為O2+4H++4e-=2H2O
科目:高中化學 來源: 題型:
【題目】向物質的量各有1mol的NH4Al(SO4)2和H2SO4混合稀溶液中逐滴加入一定量Ba(OH)2溶液,產生沉淀的量隨著Ba(OH)2 加入量的變化如圖所示。下列離子方程式書寫正確的是

A. O→A:H++SO42-+Ba2++OH-=BaSO4↓+H2O
B. A→B:2Al3++3SO42-+3Ba2+ +6OH-=3BaSO4↓+2Al(OH)3↓
C. B→C:NH4++SO42-+Ba2+ +OH-=BaSO4↓+NH3·H2O
D. D→E:NH4++ OH-=NH3·H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將鐵粉和活性炭的混合物用NaCl溶液濕潤后,置于如圖所示裝置中,進行鐵的電化學腐蝕實驗。下列有關該實驗的說法正確的是( )

A.在此實驗過程中鐵元素被還原
B.鐵腐蝕過程中化學能全部轉化為電能
C.活性炭的存在會加速鐵的腐蝕
D.以水代替NaCl溶液,鐵不能發生吸氧腐蝕
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】新型陶瓷材料氮化硅(Si3N4)可用于制作火箭發動機中燃料的噴嘴。氮化硅可由石英、焦炭在高溫氮氣流中制取。完成下列填空:______SiO2+______C+______N2![]() ______Si3N4+______CO。
______Si3N4+______CO。
(1)試配平該化學反應方程式,將系數填寫在對應位置上。在方程式上標出電子轉移的方向和數目。____________
(2)反應中______被還原,當氧化產物比還原產物多 1mol 時,反應中電子轉移數為______。
(3)在該反應體系中:所涉及物質屬于非極性分子的電子式為______;所涉及元素中原子半徑最大的原子的最外層電子排布式為______。
(4)反應的主要產物氮化硅所屬的晶體類型為______,證明氮化硅組成元素非金屬性強弱:
(Ⅰ)寫出一個化學事實______;
(Ⅱ)從原子結構上進行說明:______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設 NA 為阿伏加德羅常數的值,下列說法錯誤的是( )
A.標準狀況下,80g SO3 所含的原子數為 4NA
B.過氧化鈉與水反應時,生成 0.1molO2 轉移的電子數為 0.2NA
C.1mol N2、3mol H2 混合反應,當生成 0.1mol NH3 時,轉移電子數目為 0.3NA
D.100mL 0.1molL-1 的 Na2S 溶液,含有的陰離子數目為 0.01NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在恒溫恒容容器中發生N2O4(g)2NO2(g),若反應物的濃度由0.1molL﹣1降到0.06molL﹣1需20s,那么由0.06molL﹣1降到0.036molL﹣1,所需反應時間為( )
A. 10 sB. 12 sC. 大于12 sD. 小于12 s
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知: (1)Fe2O3(s)+![]() C(s)=
C(s)=![]() CO2(g)+2Fe(s),ΔH=+234.1kJmol-1
CO2(g)+2Fe(s),ΔH=+234.1kJmol-1
![]() 則
則![]() 的ΔH是( )
的ΔH是( )
A.-824.4 kJmol-1B.-627.6kJmol-1C.-744.7kJmol-1D.-169.4kJmol-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知熱化學方程式:2H2(g)+O2(g) ![]() 2H2O(l) H= -571.6 kJ·mol-1,2CH3OH(l)+3O2(g)
2H2O(l) H= -571.6 kJ·mol-1,2CH3OH(l)+3O2(g) ![]() 2CO2(g)+4H2O(l) H= -1452 kJ·mol-1,H+(aq)+OH-(aq)
2CO2(g)+4H2O(l) H= -1452 kJ·mol-1,H+(aq)+OH-(aq) ![]() H2O(l) H= -57.3 kJ·mol-1。據此判斷下列說法正確的是
H2O(l) H= -57.3 kJ·mol-1。據此判斷下列說法正確的是
A. CH3OH的燃燒熱為1452 kJ·mol-1
B. 2H2(g)+O2(g) ![]() 2H2O(g) H > -571.6 kJ·mol-1
2H2O(g) H > -571.6 kJ·mol-1
C. CH3COOH(aq)+NaOH(aq) ![]() H2O(l)+CH3COONa(aq) H= -57.3 kJ·mol-1
H2O(l)+CH3COONa(aq) H= -57.3 kJ·mol-1
D. 2CH3OH(l)+O2(g) ![]() 2CO2(g)+4H2(g) H= -880.4 kJ·mol-1
2CO2(g)+4H2(g) H= -880.4 kJ·mol-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某小組利用H2C2O4溶液和酸性KMnO4溶液反應來探究“條件對化學反應速率的影響”。實驗時,先分別量取兩種溶液,然后倒入試管中迅速振蕩混合均勻,開始計時,通過測定褪色所需時間來判斷反應的快慢。該小組設計了如下的方案。
編號 | H2C2O4溶液 | 酸性KMnO4溶液 | 溫度/℃ | ||
濃度/ molL-1 | 體積/mL | 濃度/ molL-1 | 體積/mL | ||
① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
(1)已知反應后H2C2O4轉化為CO2逸出,KMnO4轉化為MnSO4,每消耗1mol H2C2O4轉移_____mol 電子。為了觀察到紫色褪去,H2C2O4與KMnO4初始的物質的量需要滿足的關系為:c(H2C2O4)∶c(KMnO4) ≥______________。
(2)探究溫度對化學反應速率影響的實驗編號是___________(填編號,下同),可探究反應物濃度對化學反應速率影響的實驗編號是_____________。
(3)實驗①測得KMnO4溶液的褪色時間為40s,忽略混合前后溶液體積的微小變化,這段時間內平均反應速率v(KMnO4)=_______________ molL-1min-1。
(4)已知50℃時c(MnO4-)~反應時間t的變化曲線如圖。若保持其他條件不變,請在答題卡坐標圖中,畫出25℃時c(MnO4-)~t的變化曲線示意圖。
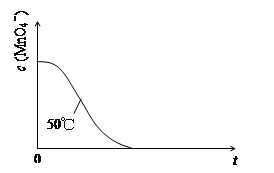 _____________
_____________
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com