
| A. | 4.6g的乙醇中含有的共價鍵的數目為0.6NA | |
| B. | 標準狀況下,22.4L CHCl3含有的原子數是5NA | |
| C. | 氫氧化燃料電池正極消耗22.4L(標準狀況)氣體時,電路中通過的電子數目為2NA | |
| D. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O反應中,生成28gN2時,轉移的電子數目為3.75NA |
分析 A.一個乙醇分子中含有共價鍵數目是8個共價鍵;
B.氣體摩爾體積適用對象為氣體;
C.燃料電池中正極發生還原反應,氫氧燃料電池中正極氧氣得到電子,1mol氧氣完全反應得到4mol;
D.5NH4NO3═2HNO3+4N2↑+9H2O中,銨根離子中N元素化合價由-3價升高為氮氣中的0價,共失去15個電子,被還原的氮元素由硝酸根中+5價降低為氮氣中的0價,共獲得15個電子.
解答 解:A.4.6g的乙醇的物質的量為$\frac{4.6g}{46g/mol}$=0.1mol,含有共價鍵0.8mol,數目為0.8NA,故A錯誤;
B.標況下,三氯甲烷為液體,不能使用氣體摩爾體積,故B錯誤;
C.燃料電池中正極發生還原反應,氫氧燃料電池中正極氧氣得到電子,1mol氧氣完全反應得到4mol,通過的電子數目為4NA,故C錯誤;
D.5NH4NO3═2HNO3+4N2↑+9H2O中,銨根離子中N元素化合價由-3價升高為氮氣中的0價,共失去15個電子,被還原的氮元素由硝酸根中+5價降低為氮氣中的0價,共獲得15個電子,則生成1mol氮氣轉移電子的物質的量=$\frac{15}{4}$=3.75mol,個數為3.75NA,故D正確;
故選:D.
點評 本題考查阿伏加德羅常數的有關計算和判斷,熟練掌握公式的使用和物質的結構是解題的關鍵,注意標況下的氣體摩爾體積使用條件和適用對象,注意氧化還原反應電子得失數目的計算,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | ①②③④ | B. | ①②③ | C. | ①②④ | D. | 只有①② |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氫氧化鈉溶液與鹽酸反應 | B. | Ba(OH)2•8H2O與NH4Cl反應 | ||
| C. | 鋁片與鹽酸反應 | D. | 鈉與冷水反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
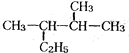
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鈾-235和碘-131是同位素 | B. | 碘-131的質子數為131 | ||
| C. | 鈾-235的中子數是143 | D. | 碘-131和銫-137是同種元素 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 的一氯取代物有5種
的一氯取代物有5種 發生加聚反應所得產物的結構簡式為
發生加聚反應所得產物的結構簡式為 .
.
 在上述類似條件下發生反應,請模仿上例寫出該反應的方程式:
在上述類似條件下發生反應,請模仿上例寫出該反應的方程式: .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 A是一種紅棕色金屬氧化物,B、D是常見金屬單質,J是一種難溶于水的白色化合物,受熱后容易發生分解.
A是一種紅棕色金屬氧化物,B、D是常見金屬單質,J是一種難溶于水的白色化合物,受熱后容易發生分解. 查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com