

分析 (1)A、B、C、D四種短周期主族元素,其原子序數依次增大,A、B可形成A2B和A2B2兩種化合物,可能為H2O、H2O2或Na2O、Na2O2,則A為H元素,B為O元素,B、C同主族且可形成CB2和CB3兩種化合物,應為SO2和SO3,則C為S元素,D應為Cl元素;
(2)非金屬性強的非金屬單質可以置換出非金屬性弱的非金屬單質,據此寫化學方程式;
(3)CB2通入A2B2溶液中可被氧化為W,則W為H2SO4;
(4)金屬元素E是中學化學常見元素,位于元素周期表的第四周期,該元素可與D形成ED2和ED3兩種化合物,則E為Fe元素,Fe與氯化鐵反應生成氯化亞鐵;
(5)石墨--鐵在氯化鐵電解質溶液中形成原電池,石墨為正極,Fe3+在正極獲得電子生成Fe2+,Fe為負極,發生氧化反應生成Fe2+,電子由負極經導線流向正極.
解答 解:A、B、C、D四種短周期主族元素,其原子序數依次增大,A、B可形成A2B和A2B2兩種化合物,可能為H2O、H2O2或Na2O、Na2O2,則A為H元素,B為O元素,B、C同主族且可形成CB2和CB3兩種化合物,應為SO2和SO3,則C為S元素,D應為Cl元素,
(1)由上述分析可知,C為硫元素,故答案為:硫;
(2)非金屬性強的非金屬單質可以置換出非金屬性弱的非金屬單質,根據反應Cl2+H2S=S+2HCl可知,非金屬性S<Cl,
故答案為:Cl2+H2S=S+2HCl;
(3)金屬元素E是中學化學常見元素,位于元素周期表的第四周期,該元素可與D形成ED2和ED3兩種化合物,則E為Fe元素,Fe與氯化鐵反應生成氯化亞鐵,該反應離子方程式為:Fe+2Fe3+=3Fe2+,
故答案為:Fe+2Fe3+=3Fe2+;
(4)石墨--鐵在氯化鐵電解質溶液中形成原電池,石墨為正極,Fe3+在正極上得電子被還原,電極反應式為:2Fe3++2e-=2Fe2+,鐵做負極,負極反應式為Fe-2e-=Fe2+,電子由負極經導線流向正極,該原電池裝置圖為: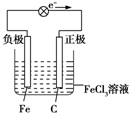 ,故答案為:Fe-2e-=Fe2+;
,故答案為:Fe-2e-=Fe2+; .
.
點評 本題考查元素推斷和原電池、常用化學用語,題目難度中等,注意正確推斷元素的種類為解答該題的關鍵,注意原電池裝置圖的繪畫.


 計算高手系列答案
計算高手系列答案科目:高中化學 來源: 題型:解答題
 如圖是實驗室制備SO2并驗證SO2某些性質的裝置圖.
如圖是實驗室制備SO2并驗證SO2某些性質的裝置圖.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 測定序號 | 待測溶液的體積/mL | 所耗鹽酸標準液的體積/mL | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.52 |
| 2 | 20.00 | 1.20 | 21.18 |
| 3 | 20.00 | 0.80 | 24.20 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 對空氣進行降溫加壓 | B. | 金剛石變成石墨 | ||
| C. | NaCl熔化 | D. | 碘溶于CCl4中 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
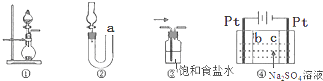
| A. | 圖①可用于實驗室制取少量NH3或O2 | |
| B. | 可用從a處加水的方法檢驗圖②裝置的氣密性 | |
| C. | 實驗室可用圖③的方法除去Cl2中混有的HCl | |
| D. | 利用圖④裝置制硫酸和氫氧化鈉,其中b為陽離子交換膜 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
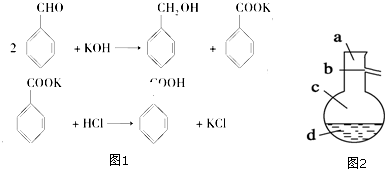
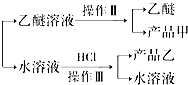
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
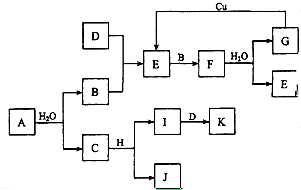 A~K為中學化學的常見物質,它們之間有如下圖所示的轉化關系(反應條件已略去).已知:通常狀況下,A是淡黃色固體,B、D和I都是無色氣體單質,F是紅棕色氣體,H是金屬單質.回答下列問題:
A~K為中學化學的常見物質,它們之間有如下圖所示的轉化關系(反應條件已略去).已知:通常狀況下,A是淡黃色固體,B、D和I都是無色氣體單質,F是紅棕色氣體,H是金屬單質.回答下列問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com