
| A. | GQXYZ | B. | XYGQZ | C. | GYQZX | D. | GXQYZ |
分析 G、Q、X、Y、Z均為氯的含氧化合物,根據氧化還原反應中Cl元素的化合價升降來分析,氧化還原反應中元素的化合價有升高,則必然有降低,以此來解答.
解答 解:①G→Q十NaCl中,NaCl中Cl元素為-1價,則Cl元素的化合價為Q>G>-1,
③Y十NaOH→G十Q十H2O中,結合①可知Cl元素的化合價為Q>Y>G,
②Q+H2O→X+H2中,H元素的化合價降低,則Cl元素的化合價升高,所以Cl元素的化合價為X>Q,
④Z十NaOH→Q十X十H2O中,結合②可知,Cl元素的化合價為X>Z>Q,
所以五種化合物中氯的化合價由低到高的順序為GYQZX,
故選C.
點評 本題考查氧化還原反應,明確氧化還原反應中元素的化合價變化是解答本題的關鍵,題目難度不大.


 全優點練單元計劃系列答案
全優點練單元計劃系列答案科目:高中化學 來源: 題型:選擇題
| A. | 只有Na2O | B. | 只有Na2O2 | C. | Na2O2和Na2O | D. | 無法確定 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 選用試劑 | 實驗現象 | |
| 方案1 | ||
| 方案2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CuS<Cu(OH)2<CuCO3 | B. | CuCO3<Cu(OH)2<CuS | C. | CuS<CuCO3<Cu(OH)2 | D. | Cu(OH)2<CuCO3<CuS |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
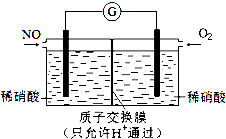 NO和NO2是常見的氮氧化物,研究它們的綜合利用有重要意義.
NO和NO2是常見的氮氧化物,研究它們的綜合利用有重要意義.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 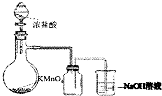 實驗室制取并收集Cl2 | B. | 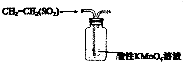 檢驗乙烯中是否含有SO2 | ||
| C. | 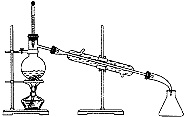 分離Br2和H20的混合物 | D. | 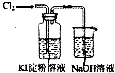 驗證氧化性Cl>I2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com