
| A. | 用A表示的反應速率是0.4 mol/(L•min) | |
| B. | 用C表示的反應速率是0.2 mol/(L•s) | |
| C. | 2 min末的反應速率,用B表示是0.3 mol/(L•min) | |
| D. | 2 min內,用B和C表示的反應速率之比為2:3 |
分析 A.化學反應速率表示單位時間內濃度的變化量,計算B的反應速率,反應速率之比等于化學方程式計量數之比;
B.根據v(C)=$\frac{△c(C)}{△t}$計算;
C.化學反應速率為一段時間內平均速率,不是即時速率;
D.反應速率之比等于化學方程式計量數之比.
解答 解:A.經2min,B的濃度減少了0.6mol/L,v(B)=$\frac{0.6mol/L}{2min}$=0.3mol/(L•min),v(A)=$\frac{4}{3}$v(B)=$\frac{4}{3}$×0.3mol/(L•min)=0.4 mol/(L•min),故A正確;
B.用C表示的反應速率是v(C)=$\frac{2}{3}$×0.3mol/(L•min)=0.2 mol/(L•min),故B錯誤;
C.2 min末的反應速率是即時速率,不是平均速率,故C錯誤;
D.2 min內,用B和C表示的反應速率之比=0.3mol/(L•min):0.2 mol/(L•min)=3:2,故D錯誤;
故選A.
點評 本題考查對化學反應速率的理解及有關計算,題目難度不大,化學反應速率為一段時間內平均速率,不是即時速率.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:選擇題
| A. | Fe2O3溶于過量的氫碘酸中:Fe2O3+6H+=2Fe3++3H2O | |
| B. | 氯化鋁溶液中加入足量的氨水:Al3++3OH-=Al(OH)3↓ | |
| C. | FeBr2溶液中加入過量的氯水:2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl- | |
| D. | 鋁和燒堿溶液:2Al+2OH-+2H2O=2AlO2-+3H2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
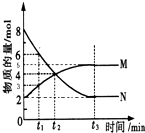 在一定溫度下,4L密閉容器內某一反應中氣體M、氣體N的物質的量隨時間變化的曲線如圖所示:
在一定溫度下,4L密閉容器內某一反應中氣體M、氣體N的物質的量隨時間變化的曲線如圖所示:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 二氧化碳與赤熱的炭反應生成一氧化碳 | |
| B. | 葡萄糖在人體內氧化分解 | |
| C. | 鋅粒與稀硫酸反應制取氫氣 | |
| D. | 氫氧化鈉與鹽酸反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com