

分析 廢電路板中加入H2O2、NH3、NH4Cl溶液,得到銅氨溶液和殘渣,分離難溶性固體和溶液采用過濾方法,所以操作①是過濾,反應Ⅰ是將Cu轉化為Cu(NH3)42+,Cu元素化合價由0價變為+2價,所以Cu是還原劑,則雙氧水是氧化劑,將Cu氧化;反應Ⅱ是銅氨溶液中的Cu(NH3)42+與有機物RH反應,生成CuR2,同時生成NH4+和NH3;
互不相溶的液體采用分液方法分離,所以操作②是分液;向有機層中加入稀硫酸,根據流程圖知,生成CuSO4和HR,然后采用分液方法分離得到HR,以石墨為電極電解CuSO4溶液時,陽極上OH-放電、陰極上Cu2+ 放電;從CuSO4溶液中獲取膽礬,采用加熱濃縮、冷卻結晶、過濾的方法得到晶體,
(1)雙氧水具有氧化性,能氧化還原性物質,分離難溶性固體和溶液采用過濾方法;
(2)反應Ⅱ是銅氨溶液中的Cu(NH3)42+與有機物RH反應生成CuR2,同時生成NH4+和NH3,根據反應物和生成物書寫該反應的離子方程式為;分離互不相溶的液體采用分液方法,分液時常用分液漏斗;
(3)反應Ⅲ是有機溶液中的CuR2與稀硫酸反應生成CuSO4和RH,分液時分液漏斗下端要緊靠燒杯內壁,且分液漏斗內不能盛放太多溶液;
(4)以石墨為電極電解硫酸銅溶液時,陽極上氫氧根離子放電、陰極上銅離子放電,SO42-向陽極移動;從溶液中獲取晶體采用加熱濃縮、冷卻結晶、過濾方法;
(5)電解硫酸銅溶液時能得到硫酸,硫酸能循環利用;氯化銨電離出的銨根離子抑制一水合氨電離而降低溶液堿性.
解答 解:廢電路板中加入H2O2、NH3、NH4Cl溶液,得到銅氨溶液和殘渣,分離難溶性固體和溶液采用過濾方法,所以操作①是過濾,反應Ⅰ是將Cu轉化為Cu(NH3)42+,Cu元素化合價由0價變為+2價,所以Cu是還原劑,則雙氧水是氧化劑,將Cu氧化;反應Ⅱ是銅氨溶液中的Cu(NH3)42+與有機物RH反應,生成CuR2,同時生成NH4+和NH3;
互不相溶的液體采用分液方法分離,所以操作②是分液;向有機層中加入稀硫酸,根據流程圖知,生成CuSO4和HR,然后采用分液方法分離得到HR,以石墨為電極電解CuSO4溶液時,陽極上OH-放電、陰極上Cu2+ 放電;從CuSO4溶液中獲取膽礬,采用加熱濃縮、冷卻結晶、過濾的方法得到晶體.
(1)雙氧水具有氧化性,能氧化還原性物質Cu,所以雙氧水作氧化劑;分離難溶性固體和溶液采用過濾方法,該混合溶液中貴重金屬是難溶物、銅氨溶液是液體,所以操作①是過濾,
故答案為:氧化劑;過濾;
(2)反應Ⅱ是銅氨溶液中的Cu(NH3)42+與有機物RH反應生成CuR2,同時生成NH4+和NH3,根據反應物和生成物書寫該反應的離子方程式Cu(NH3)42++2RH=CuR2+2NH4++2NH3↑;分離互不相溶的液體采用分液方法,分液時常用分液漏斗,分液的目的是富集銅元素、使銅元素與水溶液中的物質分離,所以ab正確,
故答案為:Cu(NH3)42++2RH=CuR2+2NH4++2NH3↑;分液漏斗;ab;
(3)反應Ⅲ是有機溶液中的CuR2與稀硫酸反應相當于復分解反應,所以生成CuSO4和RH,分液時分液漏斗下端要緊靠燒杯內壁,且分液漏斗內不能盛放太多溶液,
故答案為:RH;分液漏斗尖端未緊靠燒杯內壁;液體過多;
(4)以石墨為電極電解硫酸銅溶液時,陽極上氫氧根離子放電、陰極上銅離子放電,所以陽極上生成O2,同時有大量的H+生成,且SO42-也向陽極移動在陽極積累,因此陽極產物還有H2SO4;從溶液中獲取晶體采用加熱濃縮、冷卻結晶、過濾方法,
故答案為:O2、H2SO4;加熱濃縮、冷卻結晶、過濾;
(5)電解硫酸銅溶液時能得到硫酸,在反應III中用到硫酸,所以H2SO4能循環利用;氯化銨電離出的銨根離子抑制一水合氨電離而降低溶液堿性,從而抑制氫氧化銅生成,
故答案為:H2SO4;防止由于溶液中c(OH-)過高,生成Cu(OH)2沉淀.
點評 本題為2015年高考題,考查物質分離和提純,涉及基本實驗操作、氧化還原反應、電解原理等知識點,側重考查學生實驗操作規范性、知識綜合應用能力等,明確化學原理及基本操作原理是解本題關鍵,易錯點是硫酸是否能循環利用的判斷.


 周周清檢測系列答案
周周清檢測系列答案 輕巧奪冠周測月考直通高考系列答案
輕巧奪冠周測月考直通高考系列答案科目:高中化學 來源: 題型:選擇題
| A. | ①②④ | B. | ①③⑤ | C. | ②④⑤ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 41.8 g固體物質為Na2CO3 | |
| B. | 41.8 g固體物質為0.1 mol Na2CO3和0.4 mol Na2O2的混合物 | |
| C. | 41.8 g固體物質為31.2 g NaHCO3和10.6 g Na2CO3的混合物 | |
| D. | 一定量的Na2O2為78 g |
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
 A、B、C都是元素周期表中的短周期元素,它們的核電荷數依次增大.第2周期元素A原子的核外成對電子數是未成對電子數的2倍,B原子的最外層p軌道的電子為半滿結構,C是地殼中含量最多的元素.D是第四周期元素,其原子核外最外層電子數與氫原子相同,其余各層電子均充滿.請用對應的元素符號或化學式填空:
A、B、C都是元素周期表中的短周期元素,它們的核電荷數依次增大.第2周期元素A原子的核外成對電子數是未成對電子數的2倍,B原子的最外層p軌道的電子為半滿結構,C是地殼中含量最多的元素.D是第四周期元素,其原子核外最外層電子數與氫原子相同,其余各層電子均充滿.請用對應的元素符號或化學式填空:查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
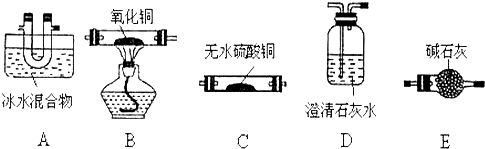
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com