
分析 (1)鋅和稀鹽酸反應生成氯化鋅和氫氣;該反應中Zn元素化合價由0價變為+2價、H元素化合價由+1價變為0價,轉移電子數為2;
(2)根據鋅和稀鹽酸關系式計算參加反應的HCl的物質的量;
(3)根據轉移電子守恒計算生成氫氣體積.
解答 解:(1)鋅和稀鹽酸反應生成氯化鋅和氫氣,反應發生為 Zn+2HCl=ZnCl2+H2↑;該反應中Zn元素化合價由0價變為+2價、H元素化合價由+1價變為0價,轉移電子數為2,電子轉移方向和數目為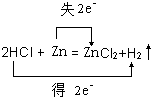 ;
;
答:反應方程式為 Zn+2HCl=ZnCl2+H2↑;電子轉移方向和數目為 ;
;
(2)根據 Zn+2HCl=ZnCl2+H2↑知,參加反應的n(HCl)=2n(Zn)=2×$\frac{6.5g}{65g/mol}$=0.2mol,
答:參加反應的稀鹽酸的物質的量是0.2mol;
(3)根據轉移電子守恒得生成氫氣體積=$\frac{\frac{6.5g}{65g/mol}×2}{2}×22.4L/mol$=2.24L,
答:生成氫氣體積是2.24L.
點評 本題考查化學反應方程式有關計算,為高頻考點,側重考查學生分析計算能力,易錯點是標電子轉移方向和數目,注意轉移電子守恒的靈活運用,題目難度不大.


科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 如圖是一個甲烷燃料電池工作時的示意圖,乙池中的兩個電極一個是石墨電極,一個是鐵電極,工作時M、N兩個電極的質量都不減少;甲池中發生的反應為:CH4+2O2+2KOH═K2CO3+3H2O.回答下列問題:
如圖是一個甲烷燃料電池工作時的示意圖,乙池中的兩個電極一個是石墨電極,一個是鐵電極,工作時M、N兩個電極的質量都不減少;甲池中發生的反應為:CH4+2O2+2KOH═K2CO3+3H2O.回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 純凈的氫氣在氯氣里安靜地燃燒,發出蒼白色火焰 | |
| B. | 氫氣與氯氣反應生成的氯化氫氣體與空氣里的水蒸氣結合,呈白霧狀 | |
| C. | 氫氣與氯氣混合后,光照發生爆炸 | |
| D. | 氫氣與氯氣的反應是化合反應,是氧化還原反應,且有電子得失 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加入鋁粉能產生H2的溶液中,可能存在大量的Na+、Ba2+、AlO2-、NO3- | |
| B. | SO2通入碘水中,反應的離子方程式為SO2+I2+2H2O═SO32-+2I-+4H+ | |
| C. | 25℃時NH4Cl溶液的KW大于100℃時NaCl溶液的KW | |
| D. | 100℃時,將pH=2的鹽酸與pH=12的NaOH溶液等體積混合,溶液顯中性 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 名稱是3,5-二甲基庚烷.
名稱是3,5-二甲基庚烷. 名稱是1,2-二甲苯.
名稱是1,2-二甲苯. 名稱是5,5-二甲基-2-己炔.
名稱是5,5-二甲基-2-己炔. 名稱是4-甲基-1-戊烯.
名稱是4-甲基-1-戊烯.查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com