
 利用Fe+CuSO4=Cu+FeSO4設計一個原電池.畫出實驗裝置圖. 并指出:
利用Fe+CuSO4=Cu+FeSO4設計一個原電池.畫出實驗裝置圖. 并指出:分析 根據原電池工作原理結合總反應方程式,還原劑作負極,不如負極活潑的金屬或非金屬導體作正極,氧化劑的溶液作電解質溶液,由此分析解答.
解答 解:不如負極活潑的金屬或導電的分金屬作正極,根據反應方程式,可選銅作正極,正極上銅離子得電子生成銅單質,電極反應式為:Cu2++2e-═Cu,而CuSO4+Fe═FeSO4+Cu,該反應中,鐵失電子生成二價鐵離子進入溶液,所以鐵作還原劑,電極反應式為:Fe-2e-═Fe2+;實驗裝置圖為: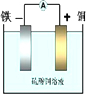 ,
,
故答案為:Cu(或C等),Cu2++2e-=Cu;Fe; Fe-2e-=Fe2+.
點評 本題考查了原電池的設計,原電池的設計關鍵是負極材料和電解質溶液的成分,一般來說,還原劑作負極,不如負極活潑的金屬或非金屬導體作正極,氧化劑的溶液作電解質溶液.


科目:高中化學 來源: 題型:選擇題
| A. | 離子化合物中一定不含共價鍵 | |
| B. | 共價化合物中一定不含離子鍵 | |
| C. | 兩種元素組成的化合物中一定不含非極性鍵 | |
| D. | 氫鍵只存在于分子之間 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 同分異構體 | B. | 不同密度的核素 | C. | 同位素 | D. | 同素異形體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 3種 | B. | 6種 | C. | 9 種 | D. | 12種 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ④①③② | B. | ①④③② | C. | ①②③④ | D. | ④③①② |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 的性質敘述不正確的是( )
的性質敘述不正確的是( )| A. | 能使溴水褪色 | |
| B. | 能使酸性高錳酸鉀溶液褪色 | |
| C. | 能發生加成反應 | |
| D. | 能發生加聚反應,且生成的聚合物也能使溴水褪色 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 增大反應物的量,化學反應速率一定加快 | |
| B. | 氣體反應體系的壓強增大,化學反應速率一定加快 | |
| C. | 與金屬鋅反應時,硫酸的濃度越大,產生H2速率越快 | |
| D. | 2molX氣體在2L的容器中反應,4s后濃度變為0.5mol•L-1,則其反應速率為0.125mol•L-1•s-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com