
分析 M是石油裂解的主要產品之一,M的氣體密度是相同條件下H2的14倍,則相對分子質量為28,應為CH2=CH2,在一定條件下與水反應得到A,則A為C2H5OH,化合物X是一種具有濃郁香味的有機物,X在酸性條件下水解得到A和B,可知X為酯類化合物,水解生成醇和酸,A和B分子中含有相同的碳原子數,則B為CH3COOH,X為CH3COOC2H5,以此解答該題.
解答 解:M是石油裂解的主要產品之一,M的氣體密度是相同條件下H2的14倍,則相對分子質量為28,應為CH2=CH2,在一定條件下與水反應得到A,則A為C2H5OH,化合物X是一種具有濃郁香味的有機物,X在酸性條件下水解得到A和B,可知X為酯類化合物,水解生成醇和酸,A和B分子中含有相同的碳原子數,則B為CH3COOH,X為CH3COOC2H5,
(1)①由以上分析可知M為CH2=CH2,故答案為:CH2=CH2;
②B為CH3COOH,含有的官能團為-COOH,為羧基,故答案為:羧基;
(2)乙酸乙酯在酸性條件下水解生成乙酸和乙醇,方程式為CH3COOC2H5+H2O$?_{△}^{濃硫酸}$CH3COOH+C2H5OH,
故答案為:CH3COOC2H5+H2O$?_{△}^{濃硫酸}$CH3COOH+C2H5OH;
(3)A為乙醇,在催化條件下反應生成乙醛,乙醛與氧氣進一步反應可生成乙酸,方程式為2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O、2CH3CHO+O2 $\stackrel{催化劑}{→}$ 2CH3COOH,
故答案為:2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O、2CH3CHO+O2 $\stackrel{催化劑}{→}$ 2CH3COOH;
(4)某有機物Y比乙烯多2個碳原子,且與乙烯物質互為同系物關系,1H核磁共振譜圖顯示有2條峰譜且面積之比為9:1,Y的結構簡式應為(CH3)3C-OH,
故答案為:(CH3)3C-OH.
點評 本題考查有機物推斷,為高考常見題型,側重于學生的分析能力的考查,注意確定烯烴M是關鍵,再結合轉化關系推斷,注意官能團的性質與轉化,難度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案 目標測試系列答案
目標測試系列答案科目:高中化學 來源: 題型:實驗題
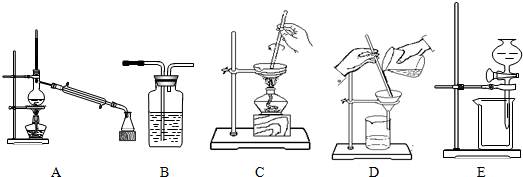
| 實驗 | 所需分離操作 |
| 1.某活動小組用海水制取粗鹽 | |
| 2.某活動小組從原油中分離出汽油、煤油等 | |
| 3.某活動小組將粗鹽溶于水,除去其不溶的泥沙 | |
| 4.某活動小組用氫氧化鈉溶液洗去CCl4中的I2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 操 作 | 現 象 |
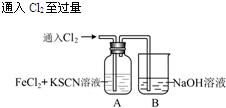 | I.A中溶液變紅 Ⅱ.稍后,溶液由紅色變為黃色 |
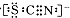
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
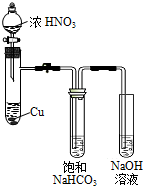 某化學學習小組發現在堿性溶液中,NO2會發生如下反應:
某化學學習小組發現在堿性溶液中,NO2會發生如下反應:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗 編號 | 反應溫度 (利用水浴加熱) | 稀硫酸 溶液 | MnSO4固體 | 0.10mol/L KMnO4溶液 | 褪色 時間 |
| 1 | 65℃ | ---- | --- | 1mL | 100s |
| 2 | 65℃ | 10滴 | --- | 1mL | 90s |
| 3 | 75℃ | 10滴 | ---- | 1mL | 40s |
| 4 | 75℃ | 10滴 | 加入少許 | 1mL | 3s |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com