
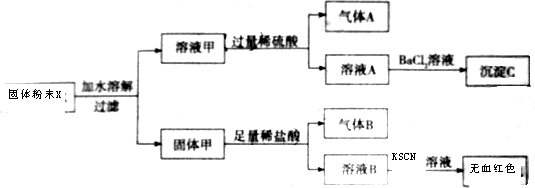
分析 K2SO3、K2CO3溶于水,且可都與稀硫酸反應生成氣體,則K2SO3、K2CO3至少一種,氣體A可能為SO2或CO2,加入硫酸鋇生成沉淀C為硫酸鋇,Fe、Fe2O3不溶于水,加入鹽酸生成氣體,則一定含有Fe,氣體B為氫氣,溶液B滴加KSN無血紅色,說明不含鐵離子,但不能說明不含Fe2O3,因Fe與鐵離子反應生成亞鐵離子,以此解答該題.
解答 解:K2SO3、K2CO3溶于水,且可都與稀硫酸反應生成氣體,則K2SO3、K2CO3至少一種,氣體A可能為SO2或CO2,加入硫酸鋇生成沉淀C為硫酸鋇,Fe、Fe2O3不溶于水,加入鹽酸生成氣體,則一定含有Fe,氣體B為氫氣,溶液B滴加KSN無血紅色,說明不含鐵離子,但不能說明不含Fe2O3,因Fe與鐵離子反應生成亞鐵離子,
(1)由以上分析可知,K2SO3、K2CO3至少一種,一定存在Fe,可能含有Fe2O3,故答案為:無;
(2)沉淀C為硫酸鋇,化學式為BaSO4,故答案為:BaSO4;
(3)固體甲與稀鹽酸反應生成氣體B的離子方程式為Fe+2H+=Fe2++H2↑,故答案為:Fe+2H+=Fe2++H2↑.
點評 本題考查物質的檢驗和鑒別的實驗方案的設計以及無機物的推斷,側重于元素化合物知識的綜合運用,題目難度中等,注意把握反應的現象,根據現象結合物質的性質進行判斷,注意體會.


 挑戰100單元檢測試卷系列答案
挑戰100單元檢測試卷系列答案 名題金卷系列答案
名題金卷系列答案科目:高中化學 來源: 題型:選擇題
| 共價鍵 | N-N | N-H | O=O | N≡N |
| 鍵能kJ•mol-1 | 3a | 2.5a | 4a | 8a |
| A. | 2a kJ•mol-1 | B. | 2.5a kJ•mol-1 | C. | 3a kJ•mol-1 | D. | 3.5a kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 水 | B. | 脂肪類物質 | C. | 淀粉類物質 | D. | 蛋白質 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 12.5% | B. | 25% | C. | <25% | D. | >25% |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 18gC含有9NA個電子 | |
| B. | 標準狀況下22.4LCCl4含有4NA個氯原子 | |
| C. | 標準狀況下,33.6LN2和H2的混合氣體中含3NA個原子 | |
| D. | 2.709×1024個原子的水分子含有1.5NA個氧原子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
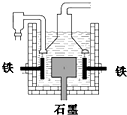 早在1807年化學家戴維用電解熔融氫氧化鈉制得鈉:
早在1807年化學家戴維用電解熔融氫氧化鈉制得鈉:| A. | 電解熔融氫氧化鈉制鈉,陽極發生電極反應為:2OH--2e-═H2↑+O2↑ | |
| B. | 蓋•呂薩克法制鈉原理是利用鐵的還原性比鈉強 | |
| C. | 若戴維法與蓋•呂薩克法制得等量的鈉,則兩反應中轉移的電子總數不相同 | |
| D. | 目前工業上常用電解熔融氯化鈉法制鈉(如上圖),電解槽中石墨極為陽極,鐵為陰極 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com