
| A. | pH=1的溶液中:Na+、K+、SO32-、MnO4- | |
| B. | pH=7的溶液中:Na+、Al3+、Cl-、SO42- | |
| C. | pH>12的溶液中:Na+、K+、SO42-、AlO2- | |
| D. | pH=0的溶液中:Na+、K+、NO3-、ClO- |
分析 A.pH=1的溶液呈酸性;
B.pH=7的溶液呈中性,水解的離子不能大量共存;
C.pH>12的溶液呈堿性;
D.pH=0的溶液呈酸性.
解答 解:A.pH=1的溶液呈酸性,酸性條件下SO32-、MnO4-發生氧化還原反應而不能大量共存,故A錯誤;
B.pH=7的溶液呈中性,Al3+水解呈酸性,不能大量共存,故B錯誤;
C.pH>12的溶液呈堿性,堿性條件下離子之間不發生任何反應,可大量共存,故C正確;
D.pH=0的溶液呈酸性,酸性條件下ClO-不能大量共存,故D錯誤.
故選C.
點評 本題考查離子的共存,為高考高頻考點,側重復分解反應、氧化還原反應的離子共存的考查,注意把握習題中的信息及常見離子之間的反應,題目難度不大.


科目:高中化學 來源: 題型:實驗題
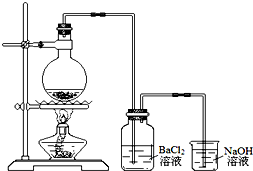 某學習小組探究銅跟濃硫酸反應的情況.取6.4g銅片和10mL 18mol•L-1的濃硫酸放在圓底燒瓶中,按如圖所示裝置進行實驗.
某學習小組探究銅跟濃硫酸反應的情況.取6.4g銅片和10mL 18mol•L-1的濃硫酸放在圓底燒瓶中,按如圖所示裝置進行實驗.查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
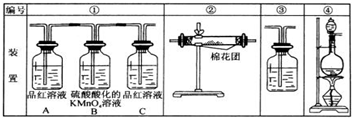
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H2SO4(aq) | B. | HCl(aq) | C. | Fe2(SO4)3(aq) | D. | CuSO4(aq) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
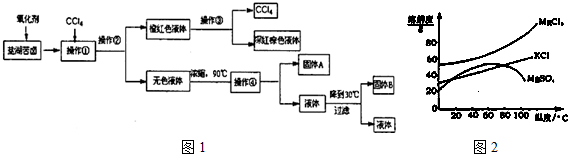
| 化學式 | BaCO3 | BaSO4 | Ca(OH)2 | MgCO3 | Mg(OH)2 |
| Ksp | 8.1×10一9 | 1.08×10一10 | 1.0×10一4 | 3.5×10一5 | 1.6×10一11 |
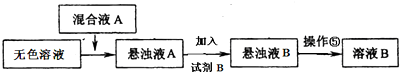
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將25gKCl溶液蒸干得到5gKCl固體,則原溶液中溶質的質量分數為20% | |
| B. | 某物質中只含有一種元素,則該物質一定是純凈物 | |
| C. | 只有一種元素的陽離子和一種元素的陰離子構成的物質一定是純凈物 | |
| D. | 鹽形成的溶液中,既不能電離出H+,也不能電離出OH- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1:1 | B. | <1:1 | C. | ≥1:1 | D. | 任意比 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com