
 Na2S2O3是重要的化工原料,易溶于水,在中性或堿性環境中穩定.
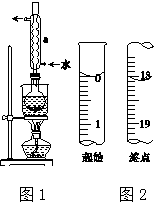
Na2S2O3是重要的化工原料,易溶于水,在中性或堿性環境中穩定.分析 (1)硫粉難溶于水、微溶于乙醇,乙醇濕潤可以使硫粉易于分散到溶液中;
(2)根據圖示裝置中儀器構造寫出其名稱,然后根據冷凝管能夠起到冷凝回流的作用進行解答;
(3)由于S2O32?具有還原性,易被氧氣氧化成硫酸根離子可知雜質為硫酸鈉;根據檢驗硫酸根離子的方法檢驗雜質硫酸鈉;
(4)S2O32?與氫離子在溶液中能夠發生氧化還原反應生成硫單質,據此寫出反應的離子方程式;
(5)根據滴定前溶液為無色,滴定結束后,碘單質使淀粉變藍,判斷達到終點時溶液顏色變化;
(6)根據圖示的滴定管中液面讀出初讀數、終讀數,然后計算出消耗碘的標準溶液體積;根據反應2S2O32-+I2═S4O62-+2I-可知,n(S2O32-)=2n(I2),然后根據題中碘單質的物質的量計算出Na2S2O3•5H2O質量及產品的純度;
(7)根據題干信息“Na2S2O3還原性較強,在溶液中易被Cl2氧化成SO42-”及化合價升降相等寫出反應的離子方程式.
解答 解:(1)硫粉難溶于水微溶于乙醇,所以硫粉在反應前用乙醇濕潤是使硫粉易于分散到溶液中,
故答案為:使硫粉易于分散到溶液中;
(2)根據題中圖示裝置圖可知,儀器a為冷凝管,該實驗中冷凝管具有冷凝回流的作用,
故答案為:冷凝管;冷凝回流;
(3)S2O32?具有還原性,能夠被氧氣氧化成硫酸根離子,所以可能存在的雜質是硫酸鈉;檢驗硫酸鈉的方法為:取少量產品溶于過量稀鹽酸,過濾,向濾液中加BaCl2溶液,若有白色沉淀,則產品中含有Na2SO4,
故答案為:Na2SO4; 取少量產品溶于過量稀鹽酸,過濾,向濾液中加BaCl2溶液,若有白色沉淀,則產品中含有Na2SO4;
(4)S2O32?與氫離子發生氧化還原反應生成淡黃色硫單質,反應的離子方程式為:S2O32?+2H+=S↓+SO2↑+H2O,
故答案為:S2O32?+2H+=S↓+SO2↑+H2O;
(5)滴定結束后,碘單質使淀粉變藍,所以滴定終點時溶液顏色變化為:由無色變為藍色,
故答案為:由無色變為藍色;
(6)根據圖示的滴定管中液面可知,滴定管中初始讀數為0,滴定終點液面讀數為18.10mL,所以消耗碘的標準溶液體積為18.10mL;
根據反應2S2O32-+I2═S4O62-+2I-可知,n(S2O32-)=2n(I2),所以W g產品中含有Na2S2O3•5H2O質量為:0.1000 mol•L-1×18.10×10-3L×2×M=3.620×10-3Mg,則產品的純度為:$\frac{3.620×10{\;}^{-3}Mg}{Wg}$×100%=$\frac{3.620×10{\;}^{-3}M}{W}$×100%,
故答案為:18.10;$\frac{3.620×10{\;}^{-3}M}{W}$×100%;
(7)Na2S2O3還原性較強,在溶液中易被Cl2氧化成SO42-,根據化合價升降相等配平后的離子方程式為:S2O32?+4Cl2+5H2O=2SO42?+8Cl?+10H+,
故答案為:S2O32?+4Cl2+5H2O=2SO42?+8Cl?+10H+.
點評 本題考查了化學實驗基本操作方法及常見儀器的構造、離子的檢驗方法、中和滴定存在即計算、離子方程式的書寫等知識,題目難度較大,試題涉及的題量較大,知識點較多,充分考查了學生對所學知識的掌握情況.


科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 一定條件下反應N2+3H2$?_{加熱}^{催化劑}$2NH3,達到平衡時,3v正(H2)=2v正(NH3) | |
| B. | 10mL濃度為1mol/L的鹽酸與過量的Zn粉反應,若加入適量的CH3COONa溶液,既能降低反應速率,又不影響H2的生成 | |
| C. | 將pH=a+1的氨水稀釋為pH=a的過程中,c(OH-)/c(NH3•H2O)變小 | |
| D. | 常溫下,向濃度為0.1mol/L的CH3COONa溶液中加入等體積等濃度的CH3COOH,混合溶液的pH=7 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 物質用途 | 解釋 | |
| A | 食醋浸泡水壺中的水垢 | 水垢中CaCO3溶于醋酸,酸性H2CO3>CH3COOH |
| B | 炒菜時加一點酒和醋 | 有酯類物質生成,使菜味香可口 |
| C | NaClO溶液可用作洗手液 | NaClO具有殺菌、消毒作用 |
| D | Al2O3可用作醫藥中的胃酸中和劑 | Al2O3能與胃酸反應,使胃液酸度降低 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.01mol/L NH4Al(SO4)2溶液與0.01mol•L-1Ba(OH)2溶液等體積混合NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3•H2O | |
| B. | 用惰性電極電解CuCl2溶液:2Cu2++2H2O$\frac{\underline{\;電解\;}}{\;}$2Cu+O2↑+4H+ | |
| C. | 將標準狀況下的11.2L氯氣通入200mL2mol•L-1的FeBr2溶液中,離子反應方程式為:4Fe2++6Br-+5Cl2=4Fe3++3Br2+10Cl- | |
| D. | 鐵粉中滴加少量濃硝酸:Fe+3NO3-+6H+=Fe3++3NO2↑+3H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 使用容量瓶前必須檢查容量瓶是否漏水 | |
| B. | 容量瓶用蒸餾水洗凈后,再用待配溶液潤洗 | |
| C. | 稱好的固體試樣需用紙條小心地送入容量瓶中 | |
| D. | 搖勻后發現凹液面下降,再加水至刻度線 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com