
【題目】鉛蓄電池是典型的可充型電池,它的正負極是情性材料,放電時的電池總反應式為:Pb+PbO2+4H++2SO42-![]() 2PbSO4+2H2O。請回答下列問題,放電時正極的電極反應式是________________________;正極區pH值將____(填“變大”、“變小”或“不變”);電解液中H2SO4的濃度將_____(填“變大”、“變小”或“不變”);當外電路通過1mol電子時,理論上負極板的質量___(填“增加”或“減小”)________g。
2PbSO4+2H2O。請回答下列問題,放電時正極的電極反應式是________________________;正極區pH值將____(填“變大”、“變小”或“不變”);電解液中H2SO4的濃度將_____(填“變大”、“變小”或“不變”);當外電路通過1mol電子時,理論上負極板的質量___(填“增加”或“減小”)________g。
【答案】 PbO2 +2e-+ 4H+ +2SO42-= PbSO4 + 2H2O 變大 變小 增加 48
【解析】分析:根據原電池的工作原理,即負極發生失去電子的氧化反應,正極發生得到電子的還原反應,結合總反應式解答。
詳解:根據總反應式可知放電時二氧化鉛得到電子生成硫酸鉛,則放電時正極的電極反應式是PbO2+2e-+4H++2SO42-=PbSO4+2H2O;由于正極消耗硫酸,氫離子濃度減小,則正極區pH值將變大;放電時消耗硫酸,則電解液中H2SO4的濃度將變小;負極鉛失去電子,生成硫酸鉛:Pb-2e-+SO42-=PbSO4,因此當外電路通過1mol電子時,理論上負極板的質量增加0.5mol×96g/mol=48g。


科目:高中化學 來源: 題型:
【題目】已知: 25℃、101 kPa下:① 2 Na(s) + 1/2 O2(g) = Na2O(s) △H1 = - 414 kJ / mol
② 2 Na(s) + O2(g) = Na2O2(s) △H2 = - 511 kJ / mol
下列說法正確的是
A. ①和②產物的陰陽離子個數比不相等
B. ①和②生成等物質的量的產物,轉移電子數不同
C. 常溫下Na與足量O2反應生成Na2O,隨溫度升高生成Na2O的速率逐漸加快
D. 25℃、101 kPa下,Na2O2(s) + 2 Na(s) = 2 Na2O(s) △H = -317 kJ / mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究CO2的利用對促進低碳社會的構建具有重要的意義。
(1) 在一定條件下將CO2 和H2轉化為甲醇蒸氣和水蒸氣的相關反應有:
CO2(g) +H2(g)![]() CO(g)+H2O(g) △H1=+41KJ/mol
CO(g)+H2O(g) △H1=+41KJ/mol
CO(g) +2H2(g)![]() CH3OH(g) △H2=-90KJ/mol
CH3OH(g) △H2=-90KJ/mol
則由CO2和H2轉化為甲醇蒸氣和水蒸氣的熱化學方程式為_____________________________________。
(2)在一定溫度下,向2L固定容積的密閉容器中通入2molCO2、3molH2,發生反應CO2(g) +3H2(g)![]() CH3OH(g) +H2O(g) △H3<0。測得CO2(g)和CH3OH(g)的濃度隨時間變化如圖所示。
CH3OH(g) +H2O(g) △H3<0。測得CO2(g)和CH3OH(g)的濃度隨時間變化如圖所示。
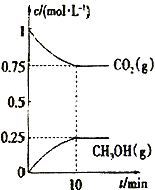
①能說明該反應已達平衡狀態的是________________________。
A.單位時間內有3n molH-H鍵斷裂,同時又有2n mol O-H鍵斷裂
B.混合氣體的密度不隨時間變化
C.體系中n(CO2)/n(H2)=1∶1,且保持不變
D. CO2的體積分數在混合氣體中保持不變
②下列措施能使n(CH3OH)/n(CO2)增大的是_______________。
A.升高溫度 B.恒溫恒容下,再充入2molCO2、3molH2
C.使用高效催化劑 D.恒溫恒容充入He使體系壓強增大
③計算該溫度下此反應的平衡常數K=_________(保留3位有效數字);若使K的值變為1,則應采取的措施是___________________________。
A.增大壓強 B.恒壓加入一定量H2 C. 升高溫度 D. 降低溫度
(3)捕捉CO2可以利用Na2CO3溶液。用100mL 0.1mol/LNa2CO3溶液完全捕捉0.44gCO2氣體(溶液體積變化不變),所得溶液中c(HCO3-)+c(CO32-)+c(H2CO3)=________ mol/L
(4)被譽為改變未來世界的十大科技之一的燃料電池是一種新型的無污染、無噪音、高效率的汽車動力和發電設備,正以勢不可擋之勢擠入汽車工業和電力工業。寫出甲醇燃料電池堿性電解質(鉑為兩極。電解液為KOH 溶液)的負極電極反應:___________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】恒溫下,將amolN2與bmH2的混合氣體通入一個固定容積的密閉容器中,發生如下反應:N2(g)+3H2(g) ![]() 2NH3(g)。
2NH3(g)。
(1)若反應進行到某時刻t時,nt(N2)=13mol,nt(NH3)=6mol,計算a的值__________。
(2)反應達平衡時,混合氣體的體積為716.8L(標準狀況下),其中NH3的含量(體積分數為25%。計算平衡時NH3的物質的量為_________________。
(3)原混合氣體與平衡混合氣體的總物質的量之比(寫最簡整數比,下同),n(始):n(平)=______。
(4)原混合氣體中,a:b=______________。
(5)達到平衡時,N2和H2的轉化率之比,a(N2):a(H2)=_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學學習了化學反應速率后,聯想到曾用H2O2制備氧氣,于是設計了下面的實驗方案并進行實驗探究。
實驗編號 | 反 應 物 | 催 化 劑 |
甲 | 試管中加入3 mL 2﹪ H2O2溶液和3滴蒸餾水 | 無 |
乙 | 試管中加入3 mL 5﹪ H2O2溶液和3滴蒸餾水 | 無 |
丙 | 試管中加入3 mL 5﹪ H2O2溶液和3滴蒸餾水 | 1 mL 0.1 mol/L FeCl3溶液 |
丁 | 試管中加入3 mL 5﹪ H2O2溶液和3滴稀鹽酸溶液 | 1 mL 0.1 mol/L FeCl3溶液 |
戊 | 試管中加入3 mL 5﹪ H2O2溶液和3滴NaOH溶液 | 1 mL 0.1 mol/L FeCl3溶液 |
【查閱資料】過氧化氫(H2O2),其水溶液俗稱雙氧水,常溫下是一種無色液體,性質比較穩定。在加熱的條件下,它能分解生成氧氣。研究表明,將新制的5﹪的H2O2溶液加熱到65℃時就有氧氣放出,加熱到80℃時就有較多氧氣產生。
(1)上述實驗發生反應的化學方程式為 。
(2)實驗甲和實驗乙的實驗目的是 ;
實驗丙、實驗丁和實驗戊的實驗目的是 。
(3)請根據該同學查閱的資料分析H2O2的性質,解釋實驗甲和實驗乙能否達到實驗目的? 。
(4)實驗過程中該同學對實驗丙、丁、戊中產生的氣體進行收集,并在2分鐘內6個時間點對注射器內氣體進行讀數,記錄數據如下表。
時間/s | 20 | 40 | 60 | 80 | 100 | 120 | |
氣體體積/mL | 實驗丙 | 9.5 | 19.5 | 29.0 | 36.5 | 46.0 | 54.5 |
實驗丁 | 8.0 | 16.0 | 23.5 | 31.5 | 39.0 | 46.5 | |
實驗戊 | 15.5 | 30.0 | 44.5 | 58.5 | 71.5 | 83.0 | |
①對實驗戊,0~20 s的反應速率v1= mL/s,100~120 s的反應速率v2= mL/s。
不考慮實驗測量誤差,二者速率存在差異的主要原因是 。
②如右圖是根據實驗收集到最大體積的氣體時所用時間繪制的圖像。曲線c表示的是實驗 (填“丙”、“丁”或“戊”)。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】電解硫酸鈉溶液聯合生產硫酸和燒堿溶液的裝置如圖所示,其中陰極和陽極均為惰性電極.測得同溫同壓下,氣體甲與氣體乙的體積比約為1:2,以下說法不正確的是( ) 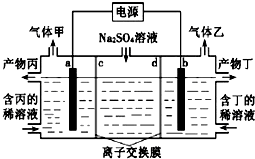
A.a極與電源的正極相連
B.產物丙為硫酸溶液
C.離子交換膜d為陽離子交換膜(允許陽離子通過)
D.a電極反應式為2H2O+2e﹣═2OH﹣+H2↑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期主族元素W、X、Y、Z的原子半徑依次增大,且X、Y原子序數之和是W、Z原子序數之和的2 倍,m、n、p、r是由這些元素組成的元化合物,甲、乙是其中兩種元素對應的單質,n 與乙均是淡黃色固體。上述物質的轉化關系如圖所示(部分反應物或生成物省略)。下列說法錯誤的是

A. 熱穩定性: p<r
B. X 與Y組成的化合物一定有漂白性
C. 含Y 元素的鹽溶液可能顯酸性、中性或堿性
D. Z 與W、X、Y 可形成離子化合物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某興趣小組用題圖1裝置(夾持裝置略)收集某葡萄酒中SO2 , 并對含量進行測定. 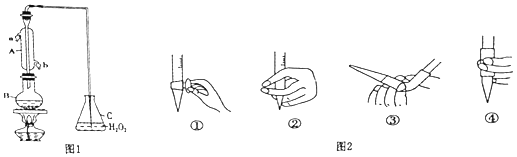
(1)儀器A的名稱是 .
(2)B中加入300.00mL葡萄酒和適量鹽酸,加熱使SO2全部逸出并與C中H2O2完全反應,其化學方程式為 .
(3)除去C中過量的H2O2 , 然后用0.0900mol/LNaOH標準溶液進行滴定,滴定前排氣泡時,應選擇圖2中的 .
(4)若滴定終點時溶液的pH=8.8,則選擇的指示劑為 .
(5)該測定結果往往比實際值偏高,分析是由于采用試劑不當引起的,可能的原因為 .
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com