
 ;1mol O22+中含有的π鍵數目為2NA.
;1mol O22+中含有的π鍵數目為2NA.| 代號 | 結構簡式 | 水中溶解度/g(25℃) | 熔點/℃ | 沸點/℃ |
| X | 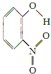 | 0.2 | 45 | 100 |
| Y | 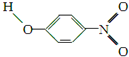 | 1.7 | 114 | 295 |
分析 (1)A.甲烷去掉一個氫原子得到甲基,不能得到CH3+、CH3-;
B.CH3+、-CH3、CH3-中價層電子對個數分別是3、4、4,根據價層電子對互斥理論判斷C原子雜化類型;
C.CH3-與NH3、H3O+均具有10個電子,互為等電子體,結構相似;
D.CH3+中的碳原子價層電子對個數是3,根據價層電子對互斥理論判斷C原子雜化類型;
(2)等電子體的結構相似,根據氮氣電子式書寫O22+電子式,每個O22+含有2個π鍵;
(3)分子間氫鍵導致物質的熔沸點升高,分子內氫鍵導致物質的熔沸點降低.
解答 解:(1)A.甲烷分子變成CH3+、-CH3、CH3-時,失去的分別是氫負離子、氫原子和氫離子,空間構型也不再與原來的分子相同,故A錯誤;
B.CH3+、-CH3、CH3-中價層電子對個數分別是3、4、4,根據價層電子對互斥理論知,C原子雜化類型分別是sp2、sp3、sp3,故B錯誤;
C.CH3-與NH3、H3O+均具有8個價電子,4個原子,互為等電子體,結構相似,氨氣分子是三角錐形結構,所以這幾種微粒都是三角錐形,故C正確;
D.CH3+中的碳原子采取sp2雜化,平面三角形結構,所有原子均共面,故D正確;
故選CD;
(2)根據等電子體的結構相似,O22+的電子式  ,在1個O22+含有2個π鍵,故1 mol O22+中,含有2NA個 π鍵,
,在1個O22+含有2個π鍵,故1 mol O22+中,含有2NA個 π鍵,
故答案為: ;2NA;
;2NA;
(3)X物質形成分子內氫鍵,物質的熔沸點降低,Y物質形成分子間氫鍵,物質的熔沸點升高,
故答案為:X物質形成分子內氫鍵,Y物質形成分子間氫鍵.
點評 本題考查原子雜化方式判斷、氫鍵、等電子體等知識點,側重考查基本理論、基本概念,會利用價層電子對互斥理論判斷微粒空間構型及原子雜化方式判斷,知道氫鍵影響物理性質不影響化學性質,題目難度不大.


科目:高中化學 來源: 題型:解答題
| 周期 族 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
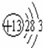 ;⑪
;⑪ .
. ;在一定條件下,若將元素①的單質和氫氣的混合氣體通入4L的密閉容器中發生反應,半分鐘后測得生成物的物質的量為1.4mol,則用元素①的單質表示的反應速率為0.35mol/(L•min).
;在一定條件下,若將元素①的單質和氫氣的混合氣體通入4L的密閉容器中發生反應,半分鐘后測得生成物的物質的量為1.4mol,則用元素①的單質表示的反應速率為0.35mol/(L•min).查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 原子半徑:A>B>C>D | B. | 原子序數:b>a>c>d | ||
| C. | 金屬性:B>A,非金屬性:D>C | D. | 離子半徑:D>C>A>B |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 經實驗測定等物質的量的鹽酸、醋酸分別與足量NaOH溶液反應放出的熱量相等 | |
| B. | 中和熱測定實驗中可以用環形鐵絲攪拌棒代替環形玻璃攪拌棒 | |
| C. | 用堿式滴定管量取0.10 mol•L-1的Na2CO3溶液22.10 mL | |
| D. | 用玻璃棒蘸取溶液滴到濕潤的廣范pH試紙上,測其pH=3.6 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加入少量MgCl2固體 | B. | 繼續加水 | ||
| C. | 加入少量Na2CO3固體 | D. | 升高溫度 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | Br2在反應中表現氧化性 | B. | SO2在反應中被還原 | ||
| C. | Br2在反應中得電子 | D. | 1mol氧化劑在反應中得到1mol電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 25℃ | B. | 1.01×103Pa | C. | 101kPa | D. | 0℃ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 實驗室制備硝基苯的反應原理和實驗裝置如下:
實驗室制備硝基苯的反應原理和實驗裝置如下: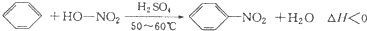
| 物質 | 熔點/℃ | 沸點/℃ | 密度/g•cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 難溶于水 |
| 間二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
| 濃硝酸 | 83 | 1.4 | 易溶于水 | |
| 濃硫酸 | 338 | 1.84 | 易溶于水 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com