

分析 (1)侯德榜制堿的原理,是飽和食鹽水中通入氨氣再通二氧化碳,反應生成氯化銨和碳酸氫鈉;
(2)煅燒生成的碳酸鈉與陶瓷的主要成份二氧化硅反應,生成硅酸鈉,所以選擇在鐵質坩堝中;濾液中有少量渾濁,可能原因有:濾紙破損、漏斗中液面高于濾紙邊緣等;
(3)從CO2在水中打的溶解度不大、而NH3極易溶于水來分析;
(4)根據最后分離出的流程,析出氯化銨得到飽和的食鹽水,分析解答.
解答 解:(1)侯德榜制堿的原理,是飽和食鹽水中通入氨氣再通二氧化碳,反應生成氯化銨和碳酸氫鈉,方程式為:NH3+H2O+CO2+NaCl=NH4Cl+NaHCO3↓,故答案為:NH3+H2O+CO2+NaCl=NH4Cl+NaHCO3↓.
(2)煅燒生成的碳酸鈉與陶瓷的主要成份二氧化硅反應,生成硅酸鈉,所以選擇在鐵質坩堝中;濾液中有少量渾濁,可能原因有:濾紙破損、漏斗中液面高于濾紙邊緣等,故答案為:鐵質;濾紙破損、濾液超過濾紙邊緣;
(3)氨氣極易溶于水,而二氧化碳微溶于水,先通入氨氣,溶液呈堿性,再通入二氧化碳氣體可之更多地轉化為HCO3-,故答案為:NH3;
(4)根據最后分離出的流程,析出氯化銨得到飽和的食鹽水,可知氯化鈉的溶解度大,故答案為:<.
點評 本題考查較為綜合,涉及食鹽的工業應用,注意把握工業制備原理和操作流程,結合物質的性質解答該題,牢固把握相關基礎知識是解答該類題目的關鍵,題目難度不大.


 全能測控一本好卷系列答案
全能測控一本好卷系列答案科目:高中化學 來源: 題型:多選題
| A. | BeCl2為共價化合物 | |
| B. | At2為無色固體,HAt不穩定,AgAt感光性強,但不溶于水也不溶于稀酸 | |
| C. | 硫酸鋇是難溶于水的白色固體 | |
| D. | 硒化氫是無色、有毒、比H2S穩定的氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該反應達到平衡時,放出的熱量等于92.4KJ | |
| B. | 達到平衡后向容器中通入1mol氦氣,平衡不移動 | |
| C. | 降低溫度和縮小容器體積均可使該反應的平衡常數增大 | |
| D. | 若達到平衡時N2的轉化率為20%,則平衡時容器內的壓強是起始時的80% |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用NaOH溶液除去CO2中混有的HCl氣體 | |
| B. | 加入適量銅粉除去Cu(NO3)2溶液中的AgNO3雜質 | |
| C. | 所有不銹鋼都只含有金屬元素 | |
| D. | 用乙醇從碘水中萃取碘 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 金屬元素A的單質不能把金屬元素B從它的鹽溶液中置換出來,一定可以說明金屬性:A<B | |
| B. | 根據反應2C+SiO2$\frac{\underline{\;高溫\;}}{\;}$Si+2CO↑,可說明C的非金屬性比Si強 | |
| C. | 周期表中第n周期第n主族的元素均為金屬 | |
| D. | 按照元素周期表的排布規律,非金屬元素最多為23種 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 與$\underset{\stackrel{16}{\;}}{8}{O}_{2}$互為同位素 | B. | 與氧氣具有相同的化學性質 | ||
| C. | 與氧氣互為同素異形體 | D. | 與同質量的氧氣具有相同的體積 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
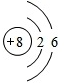 ;
;查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com