
 在實驗室里制取乙烯,常因溫度過高而使乙醇和濃硫酸反應生成少量的二氧化硫,有人設計了下列實驗圖以確認上述混合氣體中有CH2=CH2和SO2.
在實驗室里制取乙烯,常因溫度過高而使乙醇和濃硫酸反應生成少量的二氧化硫,有人設計了下列實驗圖以確認上述混合氣體中有CH2=CH2和SO2.分析 實驗室要制備純凈的乙烯并檢驗乙烯,原理為乙醇在濃硫酸做催化劑、脫水劑條件下發生消去反應,因溫度過高而使乙醇和濃硫酸反應生成少量的二氧化硫,要檢驗乙烯,借助其還原性,能夠使酸性的高錳酸鉀褪色,但是二氧化硫的存在對乙烯的檢驗造成干擾,應先檢驗二氧化硫的存在,然后除去二氧化硫,再用酸性的高錳酸鉀檢驗乙烯的存在.
(1)乙醇在濃硫酸加熱170℃發生消去反應生成乙烯氣體;
(2)I中檢驗二氧化硫用品紅溶液,II中NaOH除去二氧化硫,Ⅲ中品紅檢驗二氧化硫除盡,Ⅳ中用高錳酸鉀酸性溶液褪色檢驗乙烯;
(3)二氧化硫具有漂白性;
(4)二氧化硫、乙烯都具有還原性,都能夠使高錳酸鉀褪色;
(5)檢驗二氧化硫是否除盡;
(6)乙烯具有還原性,能夠使酸性的高錳酸鉀褪色.
解答 解:(1)乙醇在濃硫酸加熱170℃發生消去反應生成乙烯氣體化學方程式:CH3CH2OH$→_{濃硫酸}^{170℃}$CH2=CH2↑+H2O;
故答案為:CH3CH2OH$→_{濃硫酸}^{170℃}$CH2=CH2↑+H2O;
(2)I中檢驗二氧化硫用品紅溶液,II中NaOH除去二氧化硫,Ⅲ中品紅檢驗二氧化硫除盡,Ⅳ中用高錳酸鉀酸性溶液褪色檢驗乙烯;
故答案為:I A;II B;II A;IV D
(3)二氧化硫具有漂白性,能說明SO2氣體存在的現象是:裝置Ⅰ中 品紅褪色;
故答案為:裝置Ⅰ中 品紅褪色;
(4)二氧化硫、乙烯都具有還原性,都能夠使高錳酸鉀褪色,為檢驗乙烯,應除去二氧化硫;
故答案為:除去SO2以免干擾 乙烯的檢驗;
(5)使用裝置Ⅲ的目的是:檢驗SO2是否被完全除去;
故答案為:檢驗SO2是否被完全除去;
(6)乙烯具有還原性,能夠使酸性的高錳酸鉀褪色,確定含有乙烯的現象是:裝置III中品紅不褪色,裝置Ⅳ中酸性 KMnO4溶液褪色;
故答案為:裝置III中品紅不褪色,裝置Ⅳ中酸性 KMnO4溶液褪色.
點評 本題考查了乙烯的實驗室制備,側重考查實驗的設計,明確實驗原理及物質的性質和除雜檢驗的方法是解題關鍵,題目難度不大.


科目:高中化學 來源: 題型:解答題
 A、B、C、D均是由短周期元素形成的四種氣體單質,E、F均為氣體,且F為紅棕色.有關的轉化關系如圖所示(反應條件均已略去):
A、B、C、D均是由短周期元素形成的四種氣體單質,E、F均為氣體,且F為紅棕色.有關的轉化關系如圖所示(反應條件均已略去):查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 PET是聚酯類合成材料,以鹵代烴為原料合成PET的線路如圖(反應中部分無機反應物及產物已省略).已知RX2(R、R′代表烴基,X代表鹵素原子)是芳香族化合物,相對分子質量為175,其中X元素的質量分數為40.6%.
PET是聚酯類合成材料,以鹵代烴為原料合成PET的線路如圖(反應中部分無機反應物及產物已省略).已知RX2(R、R′代表烴基,X代表鹵素原子)是芳香族化合物,相對分子質量為175,其中X元素的質量分數為40.6%. .
. +nHOCH2CH2OH$\stackrel{一定條件下}{→}$
+nHOCH2CH2OH$\stackrel{一定條件下}{→}$ +2nH2O.
+2nH2O.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
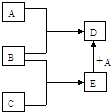 已知A、B、C、D、E均為中學化學中常見物質,在一定條件下相互轉化關系如下圖所示(反應條件和部分產物已省略).已知:
已知A、B、C、D、E均為中學化學中常見物質,在一定條件下相互轉化關系如下圖所示(反應條件和部分產物已省略).已知:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 某溫度下的溶液中,c (H+)=10x mol/L,c (OH-)=10y mol/L.
某溫度下的溶液中,c (H+)=10x mol/L,c (OH-)=10y mol/L.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
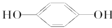 E; ③
E; ③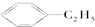 H;
H;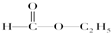 I;⑤
I;⑤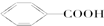 G; ⑥
G; ⑥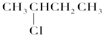 J.
J.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 時間(h) | 1 | 2 | 3 | 4 | 5 | 6 |
| P后/P前 | 0.90 | 0.85 | 0.82 | 0.81 | 0.80 | 0.80 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
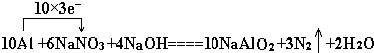
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 觀察比較外觀形態 | B. | 用手觸摸比較 | ||
| C. | 放到嘴里品嘗一下 | D. | 用化學方法進行鑒別 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com