
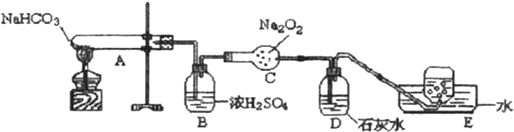
分析 實驗目的是探究碳酸氫鈉的熱穩定性,并利用其產物驗證過氧化鈉與二氧化碳的反應,由實驗裝置可知,A中碳酸氫鈉分解生成二氧化碳,B中濃硫酸干燥氣體,C中發生2Na2O2+2CO2=Na2CO3+O2,D中吸收二氧化碳,E為排水法收集氧氣,以此來解答.
解答 解:探究碳酸氫鈉的熱穩定性,并利用其產物驗證過氧化鈉與二氧化碳的反應,由實驗裝置可知,A中碳酸氫鈉分解生成二氧化碳,B中濃硫酸干燥氣體,C中發生2Na2O2+2CO2=Na2CO3+O2,D中吸收二氧化碳,E為排水法收集氧氣,
(1)A中碳酸氫鈉加熱分解生成碳酸鈉、二氧化碳氣體和水,反應的化學方程式為:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,
故答案為:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;
(2)B中濃硫酸的作用是干燥二氧化碳,
故答案為:干燥二氧化碳;
(3)C中發生反應的化學方程式為2Na2O2+2CO2=Na2CO3+O2,由O元素的化合價從-1價升高為0可知,每反應1molNa2O2轉移1mol電子,
故答案為:2Na2O2+2CO2=Na2CO3+O2;1;
(4)E中收集的氣體主要是O2,
故答案為:O2.
點評 本題考查碳酸氫鈉的性質,為高頻考點,題目難度中等,明確實驗目的為解答關鍵,注意掌握碳酸氫鈉與過氧化鈉的性質,試題側重對學生的分析能力及化學實驗能力的考查.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②③⑤ | B. | ③⑥ | C. | ③ | D. | ③⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 金屬性:Al>Mg | B. | 穩定性:HF>HCl | ||
| C. | 酸性:HClO4>H2SO4 | D. | 堿性:NaOH>Mg(OH)2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
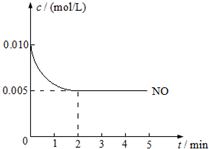 2NO(g)+O2(g)?2NO2(g)△H<0是制造硝酸的重要反應之一.在800℃時,向容積為1L的密閉容器中充入0.010mol NO和0.005molO2,反應過程中NO的濃度隨時間變化如圖所示:
2NO(g)+O2(g)?2NO2(g)△H<0是制造硝酸的重要反應之一.在800℃時,向容積為1L的密閉容器中充入0.010mol NO和0.005molO2,反應過程中NO的濃度隨時間變化如圖所示:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com