
| 編號 | 實驗操作 | 實驗現象 |
| ① | 取少量黑色粉末X放入試管1中,注入濃鹽酸,微熱 | 黑色粉末逐漸溶解,溶液呈黃綠色;有氣泡產生 |
| ② | 向試管1中滴加幾滴KSCN溶液,振蕩 | 溶液出現血紅色 |
| ③ | 另取少量黑色粉末X放入試管2中,注入足量硫酸銅溶液,振蕩,靜置 | 有極少量紅色物質析出,仍有較多黑色固體未溶解 |

分析 I.(1)極少量紅色物質為銅,該反應為鐵粉和硫酸銅反應生成銅和硫酸亞鐵,發生了金屬的置換反應.
(2)通過①③可判斷Fe的存在.再通過Ⅰ可知黑色粉末為鐵與Fe3O4.
Ⅱ.(1)通過加硝酸溶解和足量的氫氧化鈉溶液,生成了氫氧化鐵沉淀,因此操作Z為過濾;
(2)紅棕色固體為氧化鐵,根據鐵原子物質的量守恒和Fe3O4和Fe的質量為13.12g列式計算;
(3)溶液Y中鐵離子的物質的量為0.2mol,帶入c=$\frac{n}{V}$計算.
解答 解:I.(1)極少量紅色物質為銅,該反應為鐵粉和硫酸銅反應生成銅和硫酸亞鐵,發生了金屬的置換反應,離子方程式為Fe+Cu2+=Fe2++Cu,
故答案為:Fe+Cu2+=Fe2++Cu;
(2)鐵能和鹽酸反應生成氣體,且鐵和銅離子發生置換反應生成紅色的銅,據此現象判斷存在鐵;Fe3+能使KSCN溶液呈現血紅色,這是Fe3+的特征反應,據此判斷Fe3O4的存在.故黑色粉末X為Fe3O4和Fe的混合物.
故答案為:Fe3O4和Fe的混合物;
Ⅱ.(1)通過加硝酸溶解和足量的氫氧化鈉溶液,生成了氫氧化鐵沉淀,因此操作Z為過濾,
故答案為:過濾;
(2)紅棕色固體為氧化鐵,16g氧化鐵中含有鐵原子的物質的量為$\frac{16g}{160g/mol}$×2=0.2mol,設13.12g混合固體中鐵的物質的量為xmol,Fe3O4的物質的量為ymol,則
①x+3y=0.2mol②56x+232y=13.12 兩式聯立求得x=0.11mol,y=0.03mol,
故答案為:Fe:0.11mol、Fe3O4:0.03mol;
(3)通過(2)中計算可知鐵離子的物質的量為0.2mol,因此c(Fe3+)=$\frac{0.2mol}{0.2L}$=1mol/L,
故答案為:1.
點評 本題考查了鐵及其重要化合物的性質,涉及化學實驗基本操作、物質的量的計算等基本原理以及定量計算測定等,對知識綜合運用,考查思維能力,難度較大,清楚實驗原理、思路.


 第1卷單元月考期中期末系列答案
第1卷單元月考期中期末系列答案科目:高中化學 來源: 題型:解答題
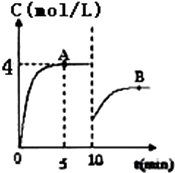 在一定條件下,合成塔中氮氣和氫氣的起始濃度分別為a mol•L-1和b mol•L-1,反應為:N2+3H2?2NH3,氨氣的濃度隨時間變化如圖所示.
在一定條件下,合成塔中氮氣和氫氣的起始濃度分別為a mol•L-1和b mol•L-1,反應為:N2+3H2?2NH3,氨氣的濃度隨時間變化如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鐵和稀鹽酸溶液反應 2Fe+6H+═2Fe2++6H2↑ | |
| B. | 醋酸和小蘇打溶液反應 CH3COOH+HCO3-═CH3COO-+H2O+CO2↑ | |
| C. | 二氧化碳和少量燒堿溶液反應 CO2+2OH-═CO32-+H2O | |
| D. | 氯化亞鐵和氯氣反應生成氯化鐵 Fe2++Cl2═Fe3++2Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 32 | B. | 32 g•mol-1 | C. | 64 g•mol-1 | D. | 64 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ${\;}_{92}^{235}$U 原子核中含有92個中子 | |
| B. | ${\;}_{92}^{235}$U 原子核外有143個電子 | |
| C. | ${\;}_{92}^{235}$U 的質量數為92 | |
| D. | ${\;}_{92}^{235}$U 與${\;}_{92}^{238}$U 互為同位素 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 焰色反應為化學變化 | |
| B. | 用完的鉑絲用稀硫酸清洗 | |
| C. | 可用焰色反應區別NaCl和KCl溶液 | |
| D. | 焰色反應為黃色,樣品一定不含鉀元素 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com