
 .
. (2)三硅酸鎂(Mg2Si3O8?nH2O)難溶于水,在醫藥上可做抗酸劑.它除了可以中和胃液中多余酸之外,生成的H2SiO3還可覆蓋在有潰瘍的胃表面,保護其不再受刺激.三硅酸鎂與鹽酸反應的化學方程式為Mg2Si3O8?nH2O+4HCl═2MgCl2+3H2SiO3+(n-1)H2O.
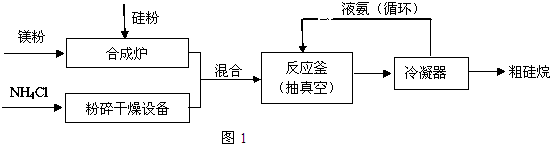
(2)三硅酸鎂(Mg2Si3O8?nH2O)難溶于水,在醫藥上可做抗酸劑.它除了可以中和胃液中多余酸之外,生成的H2SiO3還可覆蓋在有潰瘍的胃表面,保護其不再受刺激.三硅酸鎂與鹽酸反應的化學方程式為Mg2Si3O8?nH2O+4HCl═2MgCl2+3H2SiO3+(n-1)H2O.分析 根據題中流程可知,硅與鎂在合成爐中生成Mg2Si,Mg2Si與氯化銨生成粗硅烷和氨氣,經過冷凝器分離出液氨可循環使用,同時得到粗硅烷,
(1)①氯化銨中銨根離子和氯離子之間是離子鍵,銨根離子內部存在共價鍵,根據電子式的書寫方法來回答;
②根據液氨的性質:易液化來回答;
③氨氣的催化氧化產物是一氧化氮和水,一氧化氮遇到空氣迅速變為二氧化氮,二氧化到可以和水反應得到硝酸,硝酸可以和氨氣反應生成硝酸銨;
(2)三硅酸鎂中和胃酸(HCl)生成氯化鎂和硅酸,反應的化學方程式為:Mg2Si3O8?nH2O+4HCl═2MgCl2+3H2SiO3+(n-1)H2O,根據題意,被氫氧化鈉中和的鹽酸的物質的量為0.003mol,所以與三硅酸鎂反應的鹽酸為0.005mol-0.003mol=0.002mol,根據化學方程式,列比例式可計算出n的值.
解答 解:根據題中流程可知,硅與鎂在合成爐中生成Mg2Si,Mg2Si與氯化銨生成粗硅烷和氨氣,經過冷凝器分離出液氨可循環使用,同時得到粗硅烷,
(1)①氯化銨中銨根離子和氯離子之間是離子鍵,銨根離子內部存在共價鍵,極性鍵(或共價鍵)、離子鍵,硅甲烷中硅原子和氫原子之間以共價鍵結合,電子式為: ,
,
故答案為:極性鍵(或共價鍵)、離子鍵; ;
;
②液氨的性質:易液化,上述生產硅烷的過程中液氨的作用是:吸收熱量,保證反應在常溫下進行,
故答案為:吸收熱量,保證反應在常溫下進行(答“制冷”或“降溫”均可);
③氨氣的催化氧化產物是一氧化氮和水,即4NH3+5O2$\frac{\underline{催化劑}}{△}$4NO+6H2O,在實驗過程中,除觀察到錐形瓶中產生紅棕色氣體外,還可觀察到有白煙生成,因為一氧化氮遇到空氣迅速變為二氧化氮,二氧化氮可以和水反應得到硝酸,硝酸可以和氨氣反應生成硝酸銨,
故答案為:4NH3+5O2$\frac{\underline{催化劑}}{△}$4NO+6H2O;NH4NO3(或硝酸銨);
(2)三硅酸鎂中和胃酸(HCl)生成氯化鎂和硅酸,反應的化學方程式為:Mg2Si3O8?nH2O+4HCl═2MgCl2+3H2SiO3+(n-1)H2O,根據題意,被氫氧化鈉中和的鹽酸的物質的量為0.003mol,所以與三硅酸鎂反應的鹽酸為0.005mol-0.003mol=0.002mol,根據化學方程式,設0.184gMgSi3O8•nH2O的物質的量是x,得
Mg2Si3O8?nH2O+4HCl═2MgCl2+3H2SiO3+(n-1)H2O
1 4
x 0.002mol
$\frac{1}{x}$=$\frac{4}{0.002mol}$,解得x=0.0005mol,所以MgSi3O8•nH2O的摩爾質量是$\frac{0.184}{0.0005}$g/mol=368g/mol,Mg2Si3O8的摩爾質量為260g/mol,所以18n=108,即n=6.
故答案為:Mg2Si3O8?nH2O+4HCl═2MgCl2+3H2SiO3+(n-1)H2O;6.
點評 本題考查學生復雜化學時的確立方面的知識,要求學生具有分析和解決問題的能力,難度大.


科目:高中化學 來源: 題型:選擇題
| A. | Al2(SO4)3═3Al3++2SO42- | B. | AlCl3═Al3++Cl3- | ||
| C. | Mg(NO3)2═Mg2++2NO3- | D. | KMnO4═K++Mn2++4O2- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 苯甲酸 | 甲醇 | 苯甲酸甲酯 | |
| 熔點/℃ | 122.4 | -97 | -12.3 |
| 沸點/℃ | 249 | 64.3 | 199.6 |
| 密度/g•cm-3 | 1.2659 | 0.792 | 1.0888 |
| 水溶性 | 微溶 | 互溶 | 不溶 |

 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 不慎將酸濺到眼中,應立即用水沖洗,邊洗邊眨眼睛 | |
| B. | 不慎將濃堿溶液沾到皮膚上,要立即用大量水沖洗,然后涂上硼酸溶液 | |
| C. | 如果濃H2SO4沾到皮膚上,可立即用大量水沖洗,然后涂上硼酸溶液 | |
| D. | 如果少量酒精失火燃燒,可用濕抹布蓋滅火焰 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 工業上冶煉鈉,是通過電解氯化鈉飽和溶液 | |
| B. | 工業上冶煉鋁,如果以石墨為電極,則陽極石墨需要不斷補充 | |
| C. | 工業上冶煉鎂,是電解熔融氧化鎂 | |
| D. | 工業上精煉銅是粗銅為陰極 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 含有大量Fe3+的溶液:Na+、Mg2+、NO3-、SCN- | |
| B. | pH=1的溶液:Na+、K+、SO${\;}_{4}^{2-}$、CO${\;}_{3}^{2-}$ | |
| C. | 含有大量Al3+的溶液:Na+、NH4+、SO${\;}_{4}^{2-}$、Cl- | |
| D. | 含有大量NO3-的溶液:H+、Fe2+、SO${\;}_{4}^{2-}$、Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com