
| 苯甲酸 | 甲醇 | 苯甲酸甲酯 | |
| 熔點/℃ | 122.4 | -97 | -12.3 |
| 沸點/℃ | 249 | 64.3 | 199.6 |
| 密度/g•cm-3 | 1.2659 | 0.792 | 1.0888 |
| 水溶性 | 微溶 | 互溶 | 不溶 |

 .
.分析 (1)因苯甲酸在常溫下是固體,濃硫酸的密度又比甲醇的大,故應先將苯甲酸加入燒瓶中,再加入甲醇,最后向燒瓶中緩慢加入濃硫酸,反應時會有一定量的反應物汽化進入試管中,故試管中盛放的液體應是Na2CO3稀溶液,利用碳酸鈉固體洗去苯甲酸甲酯中過量的酸;
(2)待燒瓶內的混合物冷卻后,將試管及燒瓶中的液體轉移到分液漏斗中,使溶液在分液漏斗中充分混合,靜置,再分液,得到的有機物中主要是苯甲酸甲酯,還有溶解在其中的甲醇,據(jù)此答題;
(3)蒸餾的原理是利用液體沸點間存在較大的差異進行的,故收集苯甲酸甲酯的溫度應與其沸點相同,根據(jù)表中數(shù)據(jù),苯甲酸甲酯的沸點是199.6℃進行判斷;
(4)在其他實驗條件相同時,根據(jù)反應時間比較有、無濃硫酸存在條件下酯化反應進行的快慢.
解答 解:(1)因苯甲酸在常溫下是固體,濃硫酸的密度又比甲醇的大,甲醇易揮發(fā),甲醇的密度小,所以在燒瓶中混合有機物及濃硫酸的方法是先將一定量的苯甲酸放入燒瓶中,然后再加入甲醇,最后邊振蕩邊緩慢加入一定量的濃硫酸,利用碳酸鈉固體洗去苯甲酸甲酯中過量的酸,所以試管中盛放的液體可能是Na2CO3溶液,燒瓶中是苯甲酸與甲醇發(fā)生酯化反應生成苯甲酸甲酯,反應方程式為 ,
,
故答案為:先將一定量的苯甲酸放入燒瓶中,然后再加入甲醇,最后邊振蕩邊緩慢加入一定量的濃硫酸;Na2CO3溶液; ;
;
(2)為使混合物中的酸、醇能與Na2CO3溶液充分接觸并轉移到Na2CO3溶液中,應充分振蕩分液漏斗中的混合物,然后靜置,待液體分層后再進行分液.因苯甲酸甲酯的密度比水的密度大,故分液時苯甲酸甲酯在下層進入錐形瓶中,因沒有反應完的苯甲酸轉化為易溶于水而難溶于有機物的苯甲酸鈉,而甲醇易溶于苯甲酸甲酯,故分液后苯甲酸甲酯中最主要的雜質是甲醇,
故答案為:苯甲酸甲酯;甲醇;
(3)苯甲酸甲酯的沸點是199.6℃,用圖C裝置進行蒸餾提純時,當溫度計顯示199.6℃時,可用錐形瓶收集苯甲酸甲酯;
故答案為:199.6;
(4)在其他實驗條件相同時,根據(jù)反應時間比較有、無濃硫酸存在條件下酯化反應進行的快慢,即相同時間內兩個試管里生成有機層的厚度或兩個試管中生成相同厚度的有機層所需的時間,
故答案為:相同時間內兩個試管里生成有機層的厚度或兩個試管中生成相同厚度的有機層所需的時間.
點評 本題考查酯的性質,可以類比乙酸乙酯的制取完成,注意酯化反應的原理是酸脫羥基醇脫氫,本題難度中等.


 英語小英雄天天默寫系列答案
英語小英雄天天默寫系列答案 暑假作業(yè)安徽少年兒童出版社系列答案
暑假作業(yè)安徽少年兒童出版社系列答案科目:高中化學 來源: 題型:選擇題
| A. | 28g氮氣含有的原子數(shù)為NA | |
| B. | 32 g O2中所含的氧原子數(shù)目為2NA | |
| C. | 2.7g金屬鋁與足量鹽酸反應時失去的電子數(shù)為0.1NA | |
| D. | 標準狀況下22.4L水所含的分子數(shù)為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 A是由導熱材料制成的密閉容器,B是一耐化學腐蝕且易于傳熱的氣球.關閉K2,將等量且少量的NO2通過K1、K3分別充入A、B中,反應開始時,A、B的體積相同.已知:2NO2(g)?N2O4(g)△H<0.
A是由導熱材料制成的密閉容器,B是一耐化學腐蝕且易于傳熱的氣球.關閉K2,將等量且少量的NO2通過K1、K3分別充入A、B中,反應開始時,A、B的體積相同.已知:2NO2(g)?N2O4(g)△H<0.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
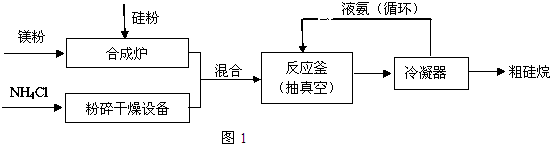
 .
. (2)三硅酸鎂(Mg2Si3O8?nH2O)難溶于水,在醫(yī)藥上可做抗酸劑.它除了可以中和胃液中多余酸之外,生成的H2SiO3還可覆蓋在有潰瘍的胃表面,保護其不再受刺激.三硅酸鎂與鹽酸反應的化學方程式為Mg2Si3O8?nH2O+4HCl═2MgCl2+3H2SiO3+(n-1)H2O.
(2)三硅酸鎂(Mg2Si3O8?nH2O)難溶于水,在醫(yī)藥上可做抗酸劑.它除了可以中和胃液中多余酸之外,生成的H2SiO3還可覆蓋在有潰瘍的胃表面,保護其不再受刺激.三硅酸鎂與鹽酸反應的化學方程式為Mg2Si3O8?nH2O+4HCl═2MgCl2+3H2SiO3+(n-1)H2O.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①④⑥ | B. | ②⑤⑦ | C. | ②④⑧ | D. | ①⑦⑧ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②④ | B. | ②④ | C. | ②③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用酒精燈給錐形瓶加熱來濃縮溶液 | |
| B. | 實驗室不能采用向下排空氣法收集CO | |
| C. | 實驗室用碳酸鈣和稀鹽酸反應,氣體產物經堿石灰干燥后可得純凈干燥的CO2 | |
| D. | 氫氧化鈣溶液存放在配有磨口塞的玻璃瓶中 |
查看答案和解析>>
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com