
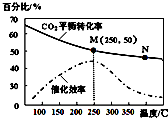
| A. | 生成乙烯的速率:v(M)有可能小于v(N) | |
| B. | 平衡常數:KM>KN | |
| C. | 當溫度高于250℃,升高溫度,平衡向逆反應方向移動,從而使催化劑的催化效率降低 | |
| D. | 若投料比n(H2):n(CO2)=3:1,則圖中M點時,乙烯的體積分數為7.7% |
分析 A、溫度升高化學反應速率加快,催化劑的催化效率降低;
B、升高溫度二氧化碳的平衡轉化率減低,則升溫平衡逆向移動;
C、根據圖象,當溫度高于250℃,升高溫度二氧化碳的平衡轉化率減低,則平衡逆向移動;
D、設開始投料n(H2)為3mol,則n(CO2)為1mol,所以當在M點平衡時二氧化碳的轉化率為50%,據此列三段式計算.
解答 解:A、化學反應速率隨溫度的升高而加快,催化劑的催化效率降低,所以v(M)有可能小于v(N),故A正確;
B、升高溫度二氧化碳的平衡轉化率減低,則升溫平衡逆向移動,所以M化學平衡常數大于N,故B正確;
C、根據圖象,當溫度高于250℃,升高溫度二氧化碳的平衡轉化率減低,則平衡逆向移動,但催化劑只影響反應速率,不影響平衡移動和轉化率,所以與催化劑的催化效率降低無因果關系,故C錯誤;
D、設開始投料n(H2)為3mol,則n(CO2)為1mol,所以當在M點平衡時二氧化碳的轉化率為50%
所以有6H2(g)+2CO2(g)$\stackrel{催化劑}{?}$CH2=CH2(g)+4H2O(g)
開始 3 1 0 0
轉化 1.5 0.5 0.25 1
平衡 1.5 0.5 0.25 1
所以乙烯的體積分數為$\frac{0.25}{1.5+0.5+0.25+1}$×100%=7.7%,故D正確;
故選C.
點評 本題考查了圖象分析化學反應速率的影響因素、平衡計算、平衡移動等,題目難度不大.


 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
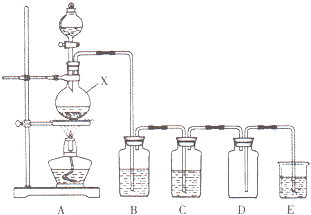 實驗室中常用二氧化錳與濃鹽酸共熱制取氯氣.某化學興趣小組為制取較為純凈、干燥的氯氣,設計了如下實驗裝置.
實驗室中常用二氧化錳與濃鹽酸共熱制取氯氣.某化學興趣小組為制取較為純凈、干燥的氯氣,設計了如下實驗裝置.查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 0~t2時,v正始終大于v逆 | |
| B. | Ⅰ、Ⅱ兩過程達到平衡時,A的體積分數Ⅰ>Ⅱ | |
| C. | Ⅰ、Ⅱ兩過程達到平衡時,平衡常數Ⅰ<Ⅱ | |
| D. | t2時刻改變的條件可以是向密閉容器中加C |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
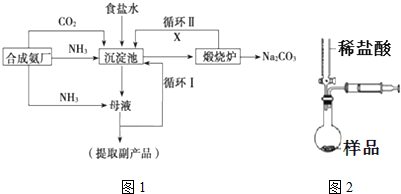
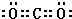 ,沉淀池中發生的化學反應方程式為:CO2+NH3+NaCl+H2O═NaHCO3↓+NH4Cl.
,沉淀池中發生的化學反應方程式為:CO2+NH3+NaCl+H2O═NaHCO3↓+NH4Cl.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 序號 | 操作及現象 | 結論 |
| A | 向2mL1mol/LNaOH溶液中先加入3滴1mol/LMgCl2溶液,再加入3滴1mol/LFeCl3 | Mg(OH)2轉化為Fe(OH)3 |
| B | 常溫下,測得飽和Na2CO3溶液的pH大于飽和NaHCO3溶液 | 常溫下水解程度:CO32->HCO3- |
| C | 向25mL冷水和沸水中分別滴入5滴FeCl3飽和溶液,前者為黃色,后者為紅褐色 | 溫度升高,Fe3+的水解程度增大 |
| D | 溴乙烷與NaOH乙醇溶液共熱產生的氣體通入KMnO4酸性溶液中,溶液褪色 | 產生的氣體為乙烯 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 煤、石油和天然氣都是重要的化石燃料 | |
| B. | 蠶絲、塑料和橡膠均屬于合成高分子材料 | |
| C. | 淀粉、麥芽糖和蛋白質均能發生水解反應 | |
| D. | 糖類、油脂和蛋白質都含有C、H、O三種元素 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com