
已知下表數據:
物質 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
完全沉淀時的pH范圍 | ≥9.6 | ≥6.4 | ≥3 |
對于含等物質的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液,下列說法正確的是
A.向該混合溶液中逐滴加入NaOH溶液,最先看到的是紅褐色沉淀
B.該溶液中c(SO42﹣):[c(Cu2+)+c(Fe2+)+c(Fe3+)]==5:4
C.向該溶液中加入適量氯水,調節pH到4~5后過濾,可獲得純凈的CuSO4溶液
D.向該溶液中加入適量氨水,調節pH到9.6后過濾,將所得沉淀灼燒,可得等物質的量的CuO、FeO、Fe2O3三種固體的混合物
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源:2016屆重慶市高三上學期第二次月考理綜化學試卷(解析版) 題型:實驗題
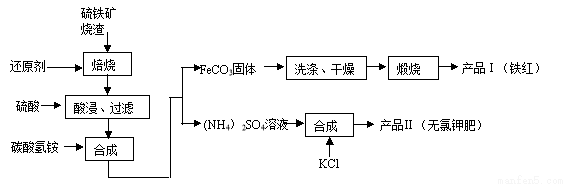
(16分)I、硫鐵礦燒渣(主要成分為Fe2O3、Fe3O4、FeO、SiO2等)是工業生產硫酸產生的廢渣,其綜合利用對環境保護具有現實意義。利用硫鐵礦燒渣制備鐵紅等產品的實驗流程如下:
已知幾種鹽的溶解度隨溫度變化的曲線如下圖所示:
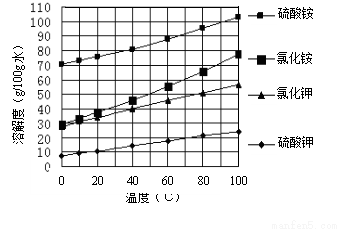
回答下列問題:
(1)酸浸、過濾后濾液中的金屬陽離子是________________。
(2)煅燒FeCO3生成產品I和CO2的化學反應方程式為 。實驗室進行煅燒操作所需儀器除了酒精燈、泥三角、三腳架、玻璃棒外,還有________________。
(3)生成產品Ⅱ的化學方程式為 。為了獲得產品Ⅱ,向(NH4)2SO4溶液中加入KCl溶液后,還需要進行的操作是: 、 、洗滌、干燥。
II、天然氣(主要成分甲烷)含有少量含硫化合物[硫化氫、羰基硫(COS)等],可以用氫氧化鈉溶液洗滌除去.羰基硫用氫氧化鈉溶液處理的過程如下(部分產物已略去):COS Na2S溶液
Na2S溶液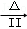 H2
H2
(4)羰基硫分子的電子式為 。反應I除生成兩種正鹽外,還有水生成,其化學方程式為 。
(5)已知反應II的產物X溶液中硫元素的主要存在形式為S2O32﹣,則II中主要反應的離子方程式為 。
(6)下圖是反應II在不同反應溫度下,反應時間與H2產量的關系圖(Na2S初始含量為3mmo1)。
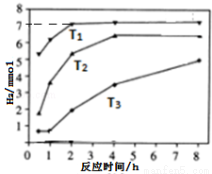
a.判斷T1、T2、T3的大小: > > ;
b.在T1溫度下,充分反應后,若X溶液中除S2O32﹣外,還有因發生副反應而同時產生的SO42﹣,則溶液中c(S2O32﹣):c(SO42﹣)= 。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北省高二9月月考化學試卷(解析版) 題型:選擇題
某反應的反應過程中能量的變化如圖所示,圖中E1表示正反應的活化能,E2表示逆反應的活化能,下列有關敘述正確的是
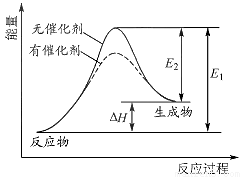
A.該反應為放熱反應
B.催化劑能改變該反應的焓變
C.E1也可表示反應物斷鍵需要吸收的總能量
D.ΔH=E2-E1
查看答案和解析>>
科目:高中化學 來源:2016屆河南省高三第二次月考化學試卷(解析版) 題型:選擇題
用NA表示阿伏加德羅常數,下列說法正確的是
A.0.2 mol H2O2完全分解轉移的電子數為0.4NA
B.300 mL 2 mol·L-1的蔗糖溶液中所含分子數為0.6NA
C.在標準狀況下,2.8g N2和2.8g CO所含電子數均為1.4NA
D.在常溫常壓下,2.24L SO2與O2混合氣體中所含氧原子數為0.2NA
查看答案和解析>>
科目:高中化學 來源:2016屆河南省三門峽市高三上學期第一次精英對抗賽化學試卷(解析版) 題型:選擇題
向100mLpH=0的硫酸和硝酸混合溶液中投入3.84g銅粉,微熱使反應充分完成后, 生成NO氣體448mL(標準狀況)。則反應前的混合溶液中含硫酸的物質的量濃度為( )
A.0.8mol·L-1 B.0.4mol·L-1 C.0.08mol·L-1 D.0.04mol·L-1
查看答案和解析>>
科目:高中化學 來源:2016屆福建省福州市高三上學期第二次質量檢測考試化學試卷(解析版) 題型:選擇題
油脂是重要的工業原料.關于“油脂”的敘述錯誤的是
A.不能用植物油萃取溴水中的溴
B.皂化是高分子生成小分子的過程
C.和H2加成后能提高其熔點及穩定性
D.水解可得到丙三醇
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北省邯鄲市高一上第一次月考化學試卷(解析版) 題型:填空題
(8分)可用于分離或提純物質的方法有:①過濾,②蒸餾,③加熱,④分液(在下列橫線上填寫分離提純的合理方法的序號)。
(1)除去石灰水中懸浮的CaCO3顆粒:________。
(2)除去NaCl晶體中混有的碘單質:________。
(3)分離汽油和煤油的混合物:________。
(4)分離水和苯的混合物:________。
查看答案和解析>>
科目:高中化學 來源:2016屆河北省冀州市高三復習班上第一次月考化學試卷A(解析版) 題型:選擇題
有一稀硫酸和稀硝酸的混合酸,其中H2SO4和HNO3的物質的量濃度分別是4 mol/L和2 mol/L,取10 mL此混合酸,向其中加入過量的鐵粉,待反應結束后,可產生標準狀況下的氣體的體積為(設反應中HNO3被還原成NO)
A.0.448 L B.0.672 L C.0.896 L D.0.224 L
查看答案和解析>>
科目:高中化學 來源:2016屆河北省衡水市高三復習班上月考化學試卷(解析版) 題型:選擇題
下列表示對應化學反應的離子方程式正確的是
A.向稀HNO3中滴加Na2SO3溶液:SO32—+2H+=SO2↑+H2O
B.向Na2SiO3溶液中通入過量SO2:SiO32—+ SO2+ H2O=H2SiO3↓+SO32—
C.向Al2(SO4)3溶液中加入過量的NH3·H2O:Al3 ++4NH3·H2O=[Al(OH)4]—+4NH4+
D.向CuSO4溶液中加入Na2O2:2 Na2O2+2Cu2++2H2O=4Na++2Cu(OH)2↓+O2↑
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com