
| A. | Q G Z Y X | B. | Z X G Y Q | C. | G Y Z Q X | D. | G Y Q Z X |
分析 G、Q、X、Y、Z均為氯的含氧化合物,物質發生歧化反應時,元素的化合價即升高又降低,結合氧化還原反應中Cl元素的化合價升降來分析解答.
解答 解:(1)G→Q十NaCl中,G中Cl元素的化合價即升高又降低,NaCl中Cl元素為-1價是最低價,則Q中Cl元素的化合價高于G中Cl元素的化合價,即Q>G>-1,
(2)Q+H20$\stackrel{電解}{→}$X+H2,電解是H元素的化合價降低,則Q中Cl元素的化合價升高,所以Cl元素的化合價為X>Q,
(3)Y十NaOH→G十Q十H2O中,Y中Cl元素的化合價即升高又降低,結合(1)可知Cl元素的化合價為Q>Y>G,
(4)Z十NaOH→Q十X十H2O中,Z中Cl元素的化合價即升高又降低,結合(2)可知,Cl元素的化合價為X>Z>Q,
所以五種化合物中氯的化合價由低到高的順序為GYQZX,
故選D.
點評 本題考查氧化還原反應,明確氧化還原反應中元素的化合價變化是解答本題的關鍵,難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 固體NaOH,存放在帶有橡皮塞的廣口瓶中,防止與空氣接觸被氧化 | |
| B. | 碳酸鈉晶體,存放在干燥密封的廣口瓶中,防止風化而碎裂成粉末 | |
| C. | 金屬鈉,存放在有水的廣口瓶中,防止氧化 | |
| D. | 過氧化鈉粉末,存放在帶玻璃塞的細口瓶中,防止吸收水分而變質 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 實驗室制取乙烯時用酸性高錳酸鉀溶液檢驗產物 | |
| B. | 除乙酸乙酯中少量的乙酸用足量氫氧化鈉溶液充分反應后分液即可 | |
| C. | 檢驗淀粉水解是否完全將水解液中加堿至堿性后加入碘水 | |
| D. | 苯、硝基苯、乙醇、乙酸四種物質只用碳酸氫鈉溶液一種試劑就能鑒別 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH3( CH2)2 CH3 和 CH3 CH=CH CH3 | |
| B. | CH3( CH2)2 CH3 和 CH3 CH2 CH( CH3) CH2 CH3 | |
| C. | CH3 C≡C CH3 和CH2=CH CH=CH2 | |
| D. | CH3 C≡C CH3 和 CH3 CH=CH CH3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 160 | B. | 160mol-1 | C. | 1600mol•L-1 | D. | 1600L•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
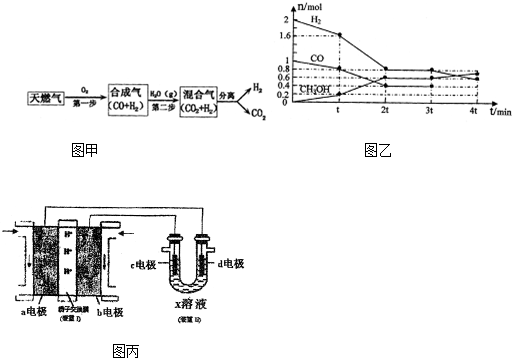
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,2.24 L CCl4所含的原子數為0.5 NA | |
| B. | 標準狀況下0.5mol NO和0.5mol O2組成的混合氣體的體積約為22.4L | |
| C. | 78 g Na2O2 與足量水反應轉移電子數為NA | |
| D. | 物質的量濃度為0.5mol/L的MgCl2溶液中,含有Cl-個數為1 NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com