
某研究性學習小組采用溫和水溶液法,以CuCl2·2H2O和H2C2O4·2H2O為原料合成新穎結構的草酸銅晶體。為進一步探究草酸銅晶體的性質,現將草酸銅晶體在一定條件下加熱分解,對所得氣體產物和紅色固體產物進行實驗和研究。

Ⅰ、用以下裝置檢驗氣體產物的成分。
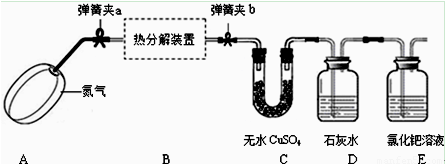
(1)C裝置的作用是檢驗 ,D裝置的作用是檢驗 。(用化學式回答)
(2)用PdCl2溶液檢驗CO時發生反應的化學方程式為______________________________;
(3)D、E兩裝置位置能否互換?為什么?_____________________________________。
(4)若需測定氣體產物的含量,則A裝置能很好地降低實驗誤差,在實驗中,至少有____次使用到A裝置,分別起什么作用?_____________________________。
Ⅱ、對固體產物的成分進行探究
①提出合理假設:
假設1:紅色固體為Cu ;
假設2:紅色固體為Cu2O ;
假設3: 。
②設計實驗方案證明你的假設(不要在答題卡上作答)
③實驗過程
根據②中方案進行實驗在答題卡上按下表的格式寫出實驗步驟、預期現象與結論。
|
實驗步驟 |
預期現象與結論 |
|
步驟1: |
|
|
步驟2: |
|
|
…… |
|
Ⅰ、(1)H2O(1分)、CO2 (1分)
(2) PdCl2 + CO + H2O = Pd↓ + CO2 + 2HCl (方程式書寫完整2分)
(3)不能,若互換則E裝置中可能產生的CO2對D裝置中CO2的檢驗造成干擾。(其他合理答案也可,2分)
(4)2 (1分)
加熱晶體前,通氮氣可除去裝置中的空氣;加熱晶體后,通氮氣可把分解產生的氣體產物全部趕出來。(其他合理答案也可,2分)
Ⅱ、①假設3:紅色固體為Cu2O和Cu的混合物。(1分)
③實驗過程(每空1分,先檢驗Cu2O、后檢驗Cu亦可)
|
實驗步驟 |
預期現象與結論 |
|
步驟1:取適量固體產物于試管中,加入足量濃氨水,充分振蕩使其溶解 |
若固體產物全部溶解,則假設2成立;若固體產物未全部溶解,則假設1或假設3成立,接著進行下一步實驗。 |
|
步驟2:另取適量固體產物于試管中,向其中加入適量稀硫酸溶液,充分振蕩 |
若溶液變藍色,結合步驟1,則假設3成立; 若溶液未變藍色,結合步驟1,則假設1成立。 |
【解析】
試題分析:Ⅰ、(1)無水硫酸銅遇水變藍,可用量檢驗H2O的存在;CO2通入石灰水變渾濁,可用石灰水檢驗CO2。
(2)根據資料卡片:CO能與PdCl2溶液反應生成黑色的鈀粉,可知PdCl2把CO氧化為CO2,配平可得方程式:PdCl2 + CO + H2O = Pd↓ + CO2 + 2HCl
(3)不能互換D、E兩裝置位置,如果顛倒順序后,E裝置產生CO2,會對D對CO2的檢驗產生干擾。
(4)2次用到A裝置,第一次:加熱晶體前,通氮氣可除去裝置中的空氣;第二次:加熱晶體后,通氮氣可把分解產生的氣體產物全部趕出來。
Ⅱ、①假設3為假設1和假設2的綜合:紅色固體為Cu2O和Cu的混合物。
③根據題目所給資料卡片:Cu2O能溶于濃氨水形成絡合物,設計步驟1:取適量固體產物于試管中,加入足量濃氨水,充分振蕩使其溶解。若固體產物全部溶解,說明只含Cu2O,則假設2成立;若固體產物未全部溶解,則假設1或假設3成立,接著進行下一步實驗。根據Cu2O與H2SO4發生歧化反應,生成CuSO4和Cu,設計步驟2:另取適量固體產物于試管中,向其中加入適量稀硫酸溶液,充分振蕩;則若溶液變藍色,結合步驟1,則假設3成立;若溶液未變藍色,結合步驟1,則假設1成立。
考點:本題考查物質的作用、方程式的書寫、實驗方案的試劑與分析評價。


科目:高中化學 來源: 題型:閱讀理解

 CO2、SO2、NOx是對環境影響較大的氣體,控制和治理CO2、SO2、NOx是解決溫室效應、減少酸雨和光化學煙霧的有效途徑.
CO2、SO2、NOx是對環境影響較大的氣體,控制和治理CO2、SO2、NOx是解決溫室效應、減少酸雨和光化學煙霧的有效途徑.
| ||
| ||
| ||
 CO+3H2
CO+3H2 CH3OH(g)+H2O(g)△H=-49.0kJ/mol,測得CO2和CH3OH(g)的濃度隨時間變化如上左圖所示.
CH3OH(g)+H2O(g)△H=-49.0kJ/mol,測得CO2和CH3OH(g)的濃度隨時間變化如上左圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解


| 1 |
| x |
| 1 |
| x |
| 3 |
| x |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
近年來,酸雨污染較為嚴重,防治酸雨成了迫在眉睫的問題。
(1)有人提出了一種利用氯堿工業產品治理含二氧化硫廢氣的方法,流程如下:
(I)將含SO2的廢氣通入電解飽和食鹽水所得溶液中,得NaHSO3溶液。
(II)將電解飽和食鹽水所得氣體反應后制得鹽酸。
(III)將鹽酸加入NaHSO3溶液中得SO2氣體回收,生成的NaCl循環利用。
①寫出步驟(I)反應的化學方程式: ;
②寫出步驟(III)反應的離子方程式: ;
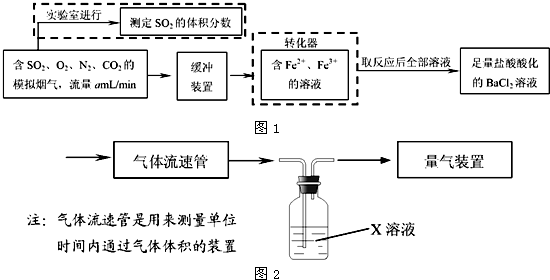
(2)某研究性學習小組采用下圖裝置在實驗室測定廢氣樣品(含SO2、O2、N2、CO2等)中SO2的體積分數,X溶液可能是 ;
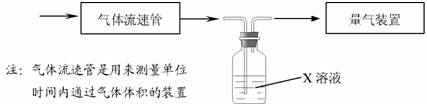
A.酸性高錳酸鉀溶液 B.氫氧化鈉溶液 C.氯化鋇溶液
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com