
| A. | 放電時,正極發生的反應是:Pb(s)+SO${\;}_{4}^{2-}$(aq)-2e-═PbSO4(s) | |
| B. | 充電時,每消耗1molPbSO4的同時轉移2mol電子 | |
| C. | 放電時,該電池的負極材料是鉛板 | |
| D. | 充電時,電池中硫酸的濃度不斷變小 |
分析 由總方程式可知,為原電池時,Pb為負極,發生氧化反應,電極方程式為Pb+SO42--2e-=PbSO4,PbO2為正極,發生還原反應,電極方程式為PbO2+4H++SO42--2e-=2H2O+PbSO4,在充電時,陰極發生的反應是PbSO4+2e-=Pb+SO42-,陽極反應為PbSO4-2e-+2H2O=PbO2+SO42-+4H+,放電時,陰離子向負極移動,陽離子向正極移動,以此解答該題.
解答 解:A.正極上二氧化鉛得電子發生還原反應,電極反應式為PbO2+4H++SO42-+2e-=PbSO4(s)+2H2O,故A錯誤;
B.根據總的電池反應,得到充電時每消耗1molPbSO4的同時轉移1mol電子,故B錯誤;
C.由總方程式可知,為原電池時,Pb為負極,發生氧化反應,故C正確.
D.由方程式可知,充電時,消耗水,生成硫酸,電解質溶液中硫酸濃度增大,故D錯誤;
故選C.
點評 本題考查原電池和電解池知識,側重于學生的分析能力和電化學知識的綜合考查,為高考常見題型和高頻考點,注意把握電解方程式的書寫,難度不大.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 鈉與水反應制氫氣 | B. | 過氧化鈉與水反應制氧氣 | ||
| C. | 氯氣與水反應制次氯酸 | D. | 氟單質與水反應制氧氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,46g的NO2和N2O4混合氣體含有的原子數為3NA | |
| B. | 將1molFeCl3水解制成膠體,所得膠體的膠粒數為NA | |
| C. | 0.5mol NH4HSO4晶體中,含有H+數目為0.5NA | |
| D. | 18gD2O含有的電子數為10NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 某溫度(t℃)下的溶液中,c(H+)=10-xmol•L-1,c(OH-)=10-ymol•L-1,x與y的關系如圖所示.請回答下列問題:
某溫度(t℃)下的溶液中,c(H+)=10-xmol•L-1,c(OH-)=10-ymol•L-1,x與y的關系如圖所示.請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1 mol Cl2完全反應轉移的電子數一定是2NA | |
| B. | 標準狀況下,22.4 L CCl4中含有的分子數為NA | |
| C. | 1 L 0.1 mol•L-1乙醇溶液中含有的氧原子數為0.1NA | |
| D. | 4 g氦氣中含有的分子數和原子數均為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
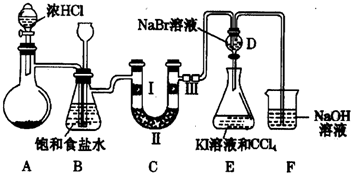
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH4分子的球棍模型: | |
| B. | 中子數為146、質子數為92的鈾原子${\;}_{92}^{146}$U | |
| C. | 氟化鈉的電子式: | |
| D. | 正丁烷的結構簡式:C4H10 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 若金屬全部溶解,則溶液中一定含有Fe3+ | |
| B. | 若金屬有剩余,向溶液中再滴入硫酸后,金屬不會發生溶解 | |
| C. | 當溶液中金屬離子只含有Fe3+、Cu2+時,則c與a、b的關系為:c=80a$\frac{1-b}{3}$ | |
| D. | 若金屬全部溶解,且產生336mL氣體(標準狀況),則c=0.3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 已知:3Fe(s)+4H2O(g)?Fe3O4(S)+4H2(g),某溫度下其平衡常數k=1.在該溫度時,在體積為5L的密閉容器中加入3mol Fe(s)與2mol H2O(g),t1秒時測得H2的物質的量為0.70mol.(計算時不用化簡)
已知:3Fe(s)+4H2O(g)?Fe3O4(S)+4H2(g),某溫度下其平衡常數k=1.在該溫度時,在體積為5L的密閉容器中加入3mol Fe(s)與2mol H2O(g),t1秒時測得H2的物質的量為0.70mol.(計算時不用化簡)查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com