
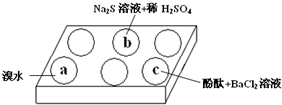
 在白色點滴板上進行Na2SO3 的性質實驗探究.如圖所示,a、b、c三個凹槽中滴有Na2SO3 溶液,再分別滴加下圖所示的試劑:
在白色點滴板上進行Na2SO3 的性質實驗探究.如圖所示,a、b、c三個凹槽中滴有Na2SO3 溶液,再分別滴加下圖所示的試劑:| n(SO3 2-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
分析 (1)Na2SO3 溶液中亞硫酸鈉具有還原性和溴單質反應生成硫酸鈉;
(2)Na2SO3 溶液與硫化鈉、硫酸溶液發生氧化還原反應生成淡黃色硫單質沉淀;
(3)Na2SO3 溶液水解顯堿性,使酚酞變紅,加入氯化鋇會結合亞硫酸根離子形成亞硫酸鋇沉淀,水解平衡逆向進行,氫氧根離子濃度減小紅色褪去;
(4)①當吸收液中n(SO32-):n(HSO3-)=10:1 時,依據圖表分析,溶液呈堿性;
A、依據溶液中電荷守恒分析;
B、溶液中亞硫酸鈉多溶液呈堿性,亞硫酸根離子大于亞硫酸氫根離子,鈉離子濃度最大;
C、溶液中亞硫酸鈉多溶液呈堿性,亞硫酸根離子大于亞硫酸氫根離子,鈉離子濃度最大;
②若n(SO32-):n(HSO3-)=3:2,直平寫出反應的離子方程式計算.
解答 解:(1)滴入溴水后褪色,說明亞硫酸鈉具有還原性,被溴單質氧化為硫酸鈉;
故答案為:溴水褪色;還原性;
(2)b中是滴入硫化鈉溶液和稀硫酸,硫離子和亞硫酸根離子發生氧化還原反應生成淡黃色沉淀單質硫,發生反應的離子方程式是:SO32-+2S2-+6H+=3S↓+3 H2O;
故答案為:SO32-+2S2-+6H+=3S↓+3 H2O;
(3)d中滴入酚酞溶液變紅,再加入BaCl2溶液后產生沉淀且紅色褪去,在Na2SO3溶液中,SO32-水解顯堿性:SO32-+H2O?HSO3-+OH-,所以滴入酚酞后溶液變紅;在該溶液中加入BaCl2后,Ba2++SO32-═BaSO3↓(白色),水解平衡左移,氫氧根離子濃度減小,紅色褪去;
故答案為:在Na2SO3溶液中,SO32-水解顯堿性:SO32-+H2O?HSO3-+OH-,所以滴入酚酞后溶液變紅;在該溶液中加入BaCl2后,Ba2++SO32-═BaSO3↓(白色),由于c(SO32-)減小,SO32-水解平衡左移,c(OH-)減小,紅色褪去;
(4)①吸收液中n(SO32-):n(HSO3-)=10:1 時,依據圖表數據分析判斷,溶液呈堿性,亞硫酸鈉物質的量大于亞硫酸氫鈉
a、依據溶液中電荷守恒,c(Na+)+c(H+)=2c(SO32-)+c(HSO3-)+c(OH-);故a正確;
b、溶液中亞硫酸鈉多溶液呈堿性,亞硫酸根離子大于亞硫酸氫根離子,鈉離子濃度最大,離子濃度大小為:c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+)
;故b錯誤;
c、溶液中亞硫酸鈉多溶液呈堿性,亞硫酸根離子大于亞硫酸氫根離子,鈉離子濃度最大,離子濃度大小為:c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+)
;故c正確;
故答案為:ac;
②若n(SO32-):n(HSO3-)=3:2,反應物全部反應,直平得到反應方程式為:5SO2+8NaOH=2NaHSO3+3Na2SO3+3H2O,則0.8mol NaOH溶液吸收了標準狀況下的SO2物質的量為0.5mol,標準狀況體積為0.5mol×22.4L/mol=11.2L;
故答案為:11.2.
點評 本題考查了物質性質實驗驗證方法的分析判斷,溶液中離子濃度大小比較,溶液中電荷守恒應用,化學方程式的計算分析,鹽類水解平衡的影響因素判斷,題目難度中等.


科目:高中化學 來源: 題型:解答題
| 時間(h) | 開始 | 8 | 16 | 24 | 32 | 40 | 48 |
| pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
| 編號 | 實驗 | 現象 |
| a | 放入蒸餾水 | 木條燃燒 |
| b | 放入Na2SiO3飽和溶液 | 木條不燃燒 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 實驗①證明KClO3具有還原性 | |
| B. | 實驗②中氧化劑與還原劑的物質的量之比為2:1 | |
| C. | 實驗③說明KI被氧化 | |
| D. | 上述實驗證明氧化性:ClO3->Cl2>I2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 編號 | T/K | 鋅規格 | 鹽酸濃度/mol•L-1 | 實驗目的 |
| ① | 298 | 粗顆粒 | 2.00 | (Ⅰ)實驗①和②探究鹽酸濃度對該反應速率的影響;(Ⅱ)實驗①和 ③探究溫度對該反應速率的影響;(Ⅲ)實驗①和 ④探究鋅規格(粗、細)對該反應速率的影響. |
| ② | 298 | |||
| ③ | 308 | |||
| ④ | 298 |
| 時間(S) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 氫氣體積(mL) | 16.8 | 39.2 | 67.2 | 224 | 420 | 492.8 | 520.8 | 543.2 | 554.4 | 560 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H+、Ba2+、ClO-、SO42- | B. | Fe3+、H+、SO42-、I- | ||
| C. | Cu2+、NO3-、HCO3-、OH- | D. | K+、Ba2+、NO3-、Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 金屬鈉著火時,立即用沾水的毛巾覆蓋 | |
| B. | 配制稀硫酸時將水倒入濃硫酸中并不斷攪拌 | |
| C. | 不慎灑出的酒精在桌上著火時,立即用水撲滅 | |
| D. | 大量氯氣泄漏時,迅速離開現場并盡量往高處去 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com