
| 編 號 | а取值范圍 | 產物化學式(離子符號) |
| ① | I2、Br- | |
| ② | $\frac{1}{6}$<а<1/5 | |
| ③ | I2、IO3-、Br2 | |
| ④ |
分析 (1)根據題干信息可知,發生反應的方程式有:KBrO3+6KI+3H2SO4═3I2+KBr+3K2SO4+3H2O、2KBrO3+10KI+6H2SO4═5I2+Br2+6K2SO4+6H2O、6KBrO3+5KI+3H2SO4═5KIO3+3Br2+3K2SO4+3H2O,根據反應方程式確定a的范圍及產物;
(2)碘單質和碘酸鉀的物質的量相等,碘單質和碘酸鉀的物質的量為:$\frac{1mol}{3}$=$\frac{1}{3}$mol,然后根據反應10KI+2KBrO3+6H2SO4=5I2+Br2+6K2SO4+6H2O和5KI+6KBrO3+3H2SO4=5KIO3+3Br2+3K2SO4+3H2O計算a值.
解答 解:(1)根據題干信息可知,發生反應的方程式有:KBrO3+6KI+3H2SO4═3I2+KBr+3K2SO4+3H2O、2KBrO3+10KI+6H2SO4═5I2+Br2+6K2SO4+6H2O、6KBrO3+5KI+3H2SO4═5KIO3+3Br2+3K2SO4+3H2O,
①當a≤$\frac{1}{6}$時,KBrO3不足,反應生成I2、Br-,反應方程式為:6KI+KBrO3+3H2SO4=3I2+KBr+3K2SO4+3H2O,則產物為:I2、Br-;
②當 $\frac{1}{6}$<a<$\frac{1}{5}$時發生反應:KBrO3+6KI+3H2SO4═3I2+KBr+3K2SO4+3H2O、2KBrO3+10KI+6H2SO4═5I2+Br2+6K2SO4+6H2O,反應產物為:I2、Br-、Br2;發生的反應具有A又有B的反應;
④當a≥$\frac{5}{6}$時,KBrO3足量,發生反應為:5KI+6KBrO3+3H2SO4=5KIO3+3Br2+3K2SO4+3H2O,所以反應產物為:IO3-、Br2;
③當 $\frac{1}{5}$<a<$\frac{5}{6}$時,反應按照反應2KBrO3+10KI+6H2SO4═5I2+Br2+6K2SO4+6H2O、6KBrO3+5KI+3H2SO4═5KIO3+3Br2+3K2SO4+3H2O進行,反應產物為:I2、IO3-、Br2,
故答案為:
| 編 號 | а 的取值范圍 | 產物的化學式(離子符號) |
| ① | a≤1/6 | I2、Br- |
| ② | 1/6<а<1/5 | I2、Br-、Br2 |
| ③ | 1/5<а<6/5 | I2、IO3-、Br2 |
| ④ | A≥6/5 | IO3-、Br2 |
點評 本題考查了有關范圍討論的化學計算,題目難度較大,根據題干信息正確判斷各物質的氧化性強弱為較大關鍵,要求學生能夠根據氧化性強弱正確書寫發生反應的化學方程式.


科目:高中化學 來源: 題型:選擇題
| A. | 一滴香: | B. | 芬必得: | ||
| C. | 維生素B5: | D. | 撲熱息痛: |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 電解時電解池的陽極一定是陰離子放電 | |
| B. | 反應NH3(g)+HCl(g)═NH4Cl(s)在室溫下可自發進行:則該反應的△H>0 | |
| C. | 其他條件不變,增大壓強,平衡可能移動,但平衡常數一定不變 | |
| D. | 鐵制品表面鑲鋅塊和鐵制品表面鍍錫,都能起到防腐的作用且防腐原理是相同的 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | FeCl3 | B. | FeCl2 | C. | Fe(OH)3 | D. | Fe3O4 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加少量NaCl固體 | B. | 加少量NaOH | C. | 加少量CuSO4固體 | D. | 加少量Na2S固體 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 開始沉淀的pH | 沉淀完全的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 )是世界上應用最廣泛的解熱、鎮痛和抗炎藥.乙酰水楊酸受熱易分解,分解溫度為128~135℃.某學習小組在實驗室以水楊酸(鄰羥基苯甲酸)與醋酸酐[(CH3CO)2O]為主要原料合成阿司匹林,制備基本操作流程如下:
)是世界上應用最廣泛的解熱、鎮痛和抗炎藥.乙酰水楊酸受熱易分解,分解溫度為128~135℃.某學習小組在實驗室以水楊酸(鄰羥基苯甲酸)與醋酸酐[(CH3CO)2O]為主要原料合成阿司匹林,制備基本操作流程如下: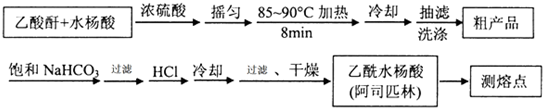
| 名稱 | 相對分子質量 | 熔點或沸點(℃) | 水 |
| 水楊酸 | 138 | 158(熔點) | 微溶 |
| 醋酸 | 102 | 139.4(沸點) | 反應 |
| 乙酸水楊酸 | 180 | 135(熔點) | 微溶 |
 .
.

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com