
| A. | 2mol/L | B. | 1.5mol/L | C. | 1mol/L | D. | 0.5mol/L |
分析 還原性Fe2+>Br-,所以通入氯氣先發生反應2Fe2++Cl2═2Fe3++2Cl-,Fe2+反應完畢,剩余的氯氣再發生反應2Br-+Cl2═Br2+2Cl-,氯氣完全反應,Cl2的物質的量=$\frac{3.36L}{22.4L/mol}$=0.15mol,若Br-沒有反應,則n(FeBr2)=0.5n(Br-)=0.15mol,0.15molFe2+只能消耗0.075mol的Cl2,故有部分Br-參加反應,設FeBr2的物質的量為x,則n(Fe2+)=x mol,n(Br-)=2x mol,未反應的n(Br-)=0.3 mol,參加反應的n(Br-)=(2x-0.3)mol,根據電子轉移守恒列方程計算x值,再根據c=$\frac{n}{V}$計算.
解答 解:還原性Fe2+>Br-,所以通入氯氣先發生反應2Fe2++Cl2═2Fe3++2Cl-,Fe2+反應完畢,剩余的氯氣再反應反應2Br-+Cl2═Br2+2Cl-,溶液中含有Br-,說明氯氣完全反應,Cl2的物質的量為$\frac{3.36L}{22.4L/mol}$=0.15mol,若Br-沒有反應,則n(FeBr2)=0.5n(Br-)=0.15mol,0.15molFe2+只能消耗0.075mol的Cl2,故有部分Br-參加反應;
設FeBr2的物質的量為x,則n(Fe2+)=x mol,n(Br-)=2x mol,未反應的n(Br-)=0.3 mol,參加反應的n(Br-)=(2x-0.3)mol,根據電子轉移守恒有x×1+[2x-0.3]×1=0.15mol×2,解得x=0.2 mol,所以原FeBr2溶液的物質的量濃度為$\frac{0.2mol}{0.1L}$=2mol/L.
故選:A.
點評 本題考查反應方程式的計算,難度中等,清楚還原性Fe2+>Br-,通入的Cl2首先氧化Fe2+,待Fe2+全部被氧化后才氧化Br-,判斷Br-是否完全反應,是解題的關鍵


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:選擇題
| A. | 合金一定是多種金屬的混合物 | B. | 合金的性能往往比純金屬優越 | ||
| C. | 合金的熔點一般比其組成金屬低 | D. | 合金的硬度一般比其組成金屬大 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 使酚酞試液變紅的溶液中:Na+、HCO3-、NO3-、SiO32- | |
| B. | 某透明溶液中:Fe3+、K+、NO3-、Cl- | |
| C. | 某溶液中加入金屬鋁有氫氣放出:K+、Ba2+、Cl-、SiO32- | |
| D. | 某無色溶液中:K+、Al3+、AlO2-、Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 堿 | 鹽 | 電解質 | 混合物 | |
| A | 純堿 | 小蘇打 | BaSO4 | 鹽酸 |
| B | 燒堿 | 食鹽 | NH3•H2O | CuSO4•5H2O |
| C | KOH | CaCO3 | 醋酸 | 水玻璃 |
| D | NH3 | Na2S | 明礬 | 磁性氧化鐵 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
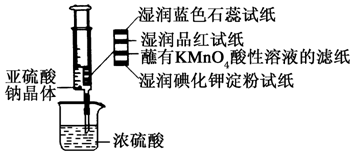 如圖所示,在注射器中加入少量Na2SO3晶體,并吸入少量濃硫酸(以不接觸紙條為準).則下列有關說法正確的是( )
如圖所示,在注射器中加入少量Na2SO3晶體,并吸入少量濃硫酸(以不接觸紙條為準).則下列有關說法正確的是( )| A. | 濕潤的藍色石蕊試紙先變紅后褪色 | |
| B. | 濕潤的品紅試紙,蘸有KMnO4酸性溶液的濾紙均褪色證明了SO2的漂白性 | |
| C. | 濕潤的碘化鉀淀粉試紙未變藍說明SO2氧化性強于I2 | |
| D. | 實驗后,可把注射器中的物質推入NaOH溶液,以減少環境污染 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 光照以后,所得混合氣體中含有0.07 molHCl | |
| B. | 光照以后,所得混合氣體體積小于原混合氣體體積(相同條件下) | |
| C. | 最終所得溶液中,NaCl和NaClO的物質的量比為5:2 | |
| D. | 最終所得溶液中,還含有0.02 molNaOH |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | FeO | B. | Fe2O3 | C. | CuO | D. | Cu2O |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com