
分析 發生反應CuSO4+2NaOH=Cu(OH)2↓+Na2SO4,根據方程式計算生成的沉淀的物質的量,反應中SO42-的物質的量未發生變化,計算出的SO42-的物質的量,通過公式C=$\frac{n}{V}$得出混合溶液中SO42-的物質的量濃度.
解答 解:(1)n(CuSO4)=C(CuSO4)•V(CuSO4)=2.0mol/L×0.1L=0.2mol
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
1 1
0.2mol n[Cu(OH)2]
n[Cu(OH)2]=0.2mol
答:兩溶液混合之后生成沉淀的物質的量為0.2mol;
(2)反應中SO42-的物質的量未發生變化
n(SO42-)=n(CuSO4)=0.2mol
C(SO42-)=$\frac{n(S{{O}_{4}}^{2-})}{V混合}$=$\frac{0.2mol}{0.1L+0.1L}$=1mol/L,
答:混合溶液中 SO42-的物質的量濃度1mol/L.
點評 本題考查學生化學反應方程式的計算以及物質的量的概念及簡單計算,題目比較簡單,屬于基礎題.


科目:高中化學 來源: 題型:選擇題
| A. | 1569.84kJ | B. | 78.584kJ | C. | 6548.6kJ | D. | 4978.88kJ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
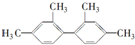 的烴,下列說法中正確的是( )
的烴,下列說法中正確的是( )| A. | 該烴苯環上的一氯取代物最多有4種 | |
| B. | 分子中至少有11個碳原子處于同一平面上 | |
| C. | 分子中至少有16個碳原子處于同一平面上 | |
| D. | 該烴屬于苯的同系物 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 對因胃酸過多而導致胃部嚴重潰瘍的病人不可使用含有碳酸氫鈉的藥物治療 | |
| B. | 淀粉、纖維素水解的最終產物都是葡萄糖 | |
| C. | 誤食了重金屬離子,應立即喝大量牛奶來緩解毒性 | |
| D. | R表示非處方藥,OTC表示處方藥 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2種 | B. | 3種 | C. | 4種 | D. | 5種 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 物質 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com