
| A. | C=$\frac{1000wρ}{M}$ | B. | w%=$\frac{CM}{1000ρ}$% | C. | C=$\frac{m}{VM}$ | D. | m=$\frac{V•ρw}{100}$ |
分析 A.根據物質的量濃度與溶質質量分數的關系c=$\frac{1000ρω}{M}$判斷;
B.根據c=$\frac{1000ρω}{M}$計算溶液質量分數或根據$\frac{溶質質量}{溶液質量}$×100%計算;
C.根據c=$\frac{n}{c}$計算溶液物質的量濃度;
D.根據m=ρV計算溶液質量,再結合質量分數計算溶質的質量,或者根據n=cV計算溶質的物質的量,再根據m=nM計算溶質的質量.
解答 解:A.根據c=$\frac{1000ρω}{M}$可知,該溶液物質的量濃度c=$\frac{1000ρ×w%}{M}$=$\frac{10ρw}{M}$,故A錯誤;
B.根據c=$\frac{1000ρω}{M}$可知,該溶液質量分數w%=$\frac{CM}{1000ρ}$=$\frac{CM}{10ρ}$%,故B錯誤;
C.溶質物質的量$\frac{m}{M}$mol,溶液物質的量濃度為$\frac{\frac{m}{M}mol}{V×1{0}^{-3}L}$=$\frac{1000m}{MV}$mol/L,故C錯誤;
D.根據m=ρV可知,溶液質量為ρVg,則溶質質量m=ρV×w%=$\frac{ρVw}{100}$,或者溶質質量m=V×10-3×C×M=VCM×10-3,故D正確,
故選D.
點評 本題考查溶液濃度有關計算,涉及物質的量濃度、質量分數計算,屬于字母型計算,為易錯題目,注意對公式的理解.


 智趣寒假作業云南科技出版社系列答案
智趣寒假作業云南科技出版社系列答案科目:高中化學 來源: 題型:選擇題
| A. | 砷在通常情況下是固體 | B. | 砷的還原性比磷弱 | ||
| C. | As2O5對應水化物的酸性比H3PO4弱 | D. | 可以存在-3、+5等多種化合價 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | FeO和HNO3 | B. | Al(OH)3與HNO3 | C. | H2S和HNO3 | D. | NH3與HNO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
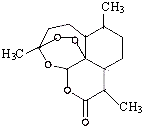 2011年9月,中國女科學家屠呦呦獲得被譽為諾貝爾獎“風向標”的拉斯克獎,這是中國醫學界迄今為止獲得的世界級最高級大獎.她獲獎理由是:“因為創制新型抗瘧藥--青蒿素和雙氫蒿素,挽救了全球特別是發展中國家的數百萬人的生命.已知青蒿素結構如圖所示,則下列說法正確的是( )
2011年9月,中國女科學家屠呦呦獲得被譽為諾貝爾獎“風向標”的拉斯克獎,這是中國醫學界迄今為止獲得的世界級最高級大獎.她獲獎理由是:“因為創制新型抗瘧藥--青蒿素和雙氫蒿素,挽救了全球特別是發展中國家的數百萬人的生命.已知青蒿素結構如圖所示,則下列說法正確的是( )| A. | 青蒿素與維生素C一樣易溶于水 | |
| B. | 青蒿素的晶體為分子晶體,其化學式為C16H20O5 | |
| C. | 青蒿素不能與NaOH溶液反應 | |
| D. | 青蒿素分子有7個手性碳原子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
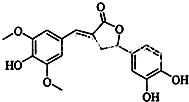
| A. | 分子中含有三種含氧官能團 | |
| B. | 1 mol 該化合物與NaOH(aq) 反應,最多消耗量4 mol NaOH | |
| C. | 既可以發生取代反應,又能夠發生加成反應 | |
| D. | 既能與FeCl3發生顯色反應,也能和NaHCO3反應放出CO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鋅錳干電池是一種常用的二次電池 | |
| B. | 氫氧燃料電池的能量轉化率可高達100% | |
| C. | 堿性鋅錳電池的正極電極反應式為MnO2+e-+H2O=MnO(OH)+OH- | |
| D. | 堿性燃料電池正極反應是O2+4e-+4H+=2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 1 mol該物質與足量溴水反應消耗6 mol Br2 | |
| B. | 1 mol該物質可與5 molNaOH反應 | |
| C. | 分子內所有原子可能在同一平面上 | |
| D. | 若能使酸性KMnO4溶液的紫色褪去,則可證明該物質分子中含有碳碳雙鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 124 g P4含有P-P鍵的個數為4NA | B. | 1mol Na2O2晶體中含離子數為4NA | ||
| C. | 22.4LCH4的分子數為NA | D. | 26g C2H2中π鍵數目為2NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com