
| A. | 該反應證明了,含最高價元素的化合物,一定具有強氧化性 | |
| B. | 1mol還原劑反應時,轉移的電子數為2NA | |
| C. | H2SO4在反應中表現了氧化性和酸性 | |
| D. | 可以利用該反應原理,將它設計成原電池,通過檢測電流強度判斷司機是否飲酒 |
分析 A.含最高價元素的化合物,不一定具有強氧化性;
B.CH3CH2OH轉化為CH3COOH,根據C元素的化合價變化分析;
C.H2SO4中沒有化合價的變化;
D.該反應是自發的氧化還原反應,可以設計為原電池.
解答 解:A.含最高價元素的化合物,不一定具有強氧化性,如HCl中H元素為+1價,是最高價,但是HCl沒有強氧化性,故A錯誤;
B.CH3CH2OH轉化為CH3COOH,C元素的化合價從-2到0價,1分子CH3CH2OH轉移4個電子,則1mol還原劑反應時,轉移的電子數為4NA,故B錯誤;
C.H2SO4中沒有化合價的變化,則H2SO4在反應中只表現了酸性,故C錯誤;
D.該反應是自發的氧化還原反應,可以設計為原電池,當乙醇的濃度越大時,電流越強,所以通過檢測電流強度判斷司機是否飲酒,故D正確.
故選D.
點評 本題考查了氧化還原反應、原電池原理,題目難度不大,注意從化合價變化的角度分析氧化還原反應,注意把握原電池反應的實質.


 全優沖刺100分系列答案
全優沖刺100分系列答案 英才點津系列答案
英才點津系列答案 紅果子三級測試卷系列答案
紅果子三級測試卷系列答案科目:高中化學 來源: 題型:選擇題
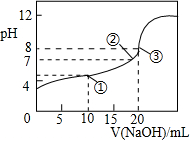 25℃時,向20.00mL0.1mol•L-1HClO2溶液中逐滴加入0.1mol•L-1的NaOH溶液.溶液的pH與滴入NaOH溶液的體積的關系如圖所示,則下列說法中不正確的是( )
25℃時,向20.00mL0.1mol•L-1HClO2溶液中逐滴加入0.1mol•L-1的NaOH溶液.溶液的pH與滴入NaOH溶液的體積的關系如圖所示,則下列說法中不正確的是( )| A. | ①點時:c(ClO2-)>c(Na+)>c(H+)>c(OH-) | |
| B. | ②點時:c(Na+)=c(ClO2-) | |
| C. | ③點時:c(H+)=c(OH-)+c(HClO2) | |
| D. | 滴定過程中可能出現:c(Na+)>c(ClO2-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 25℃時1mL水中含10-10 NA個OH-離子 | |
| B. | 1molCl2通入足量的NaOH溶液中充分反應轉移的電子數為2NA | |
| C. | a g某氣體含分子數為b,c g該氣體在標況下的體積約為22.4bc/(aNA)L | |
| D. | 0.1mol鈉和O2在一定條件下反應生成Na2O和Na2O2混合物時,失去電子數為0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NaHCO3與NaOH溶液反應:HCO3-+OH-═CO32-+H2O | |
| B. | 氯氣和水反應:Cl2+H2O?2H++Clˉ+ClOˉ | |
| C. | 氯化鐵溶液中加入足量的氨水:Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+ | |
| D. | 盛放堿性試劑的溶液不能用玻璃塞的原因:SiO2+2OH-═SiO32-+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
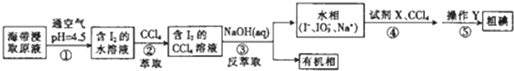
| A. | 步驟②中的萃取過程為物理變化 | |
| B. | 步驟③發生的反應中I2是氧化劑,NaOH是還原劑 | |
| C. | 步驟④所加的試劑X可能是稀硫酸 | |
| D. | 步驟⑤涉及的主要操作Y為分液和蒸餾 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

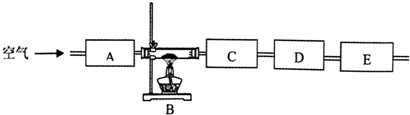
| 儀器 編號 | 藥品 | 目的 |
| A | 堿石灰 | |
| B | 綠色固體 | |
| C | ||
| D | ||
| E | 堿石灰 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 .關于它的說法正確的是( )
.關于它的說法正確的是( )| A. | 利尿酸的化學式為:C13H14O4Cl2 | |
| B. | 利尿酸最多可與4 molH2發生反應 | |
| C. | 利尿酸可使溴的四氯化碳溶液褪色 | |
| D. | 利尿酸在一定條件下能發生消去反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②③ | B. | ③④⑤ | C. | ②④⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
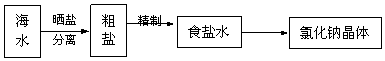
| A. | ⑤②③①⑥④⑦ | B. | ⑤①②③⑥④⑦ | C. | ⑤②①③④⑥⑦ | D. | ⑤③②①⑥④⑦ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com