
分析 Fe3+易水解,水解生成H+,方程式為:Fe3++3H2O?Fe(OH)3+3H+,依據水解方程式判斷平衡移動的方向.
解答 解:Fe3+易水解,水解生成H+,水解的離子方程式為Fe3++3H2O?Fe(OH)3+3H+,
①水解均為吸熱反應,故溫度升高,平衡右移,溶液的pH值減小;
②加少量濃鹽酸,即加入H+,導致H+濃度增大,平衡左移,但是氫離子濃度增大,pH減小;
③加水稀釋,溶液濃度變小,平衡右移,氫離子濃度減小,pH變大;
④加少量鐵粉,發生反應Fe+2Fe3+=3Fe2+,故導致Fe3+濃度減小,平衡左移,pH值增大;
⑤加少量Na2CO3(s),碳酸根與氫離子反應導致氫離子濃度減小,平衡右移,溶液的pH值增大,
依據以上分析,故答案為:(1)①③④;(2)②④;(3)①②.
點評 本題考查鹽類水解的原理及應用,題目難度不大,注意把握水解原理,學習中注重相關基礎知識的積累.


 金牌教輔培優優選卷期末沖刺100分系列答案
金牌教輔培優優選卷期末沖刺100分系列答案科目:高中化學 來源: 題型:選擇題
| A. | CO2屬于酸性氧化物 | |
| B. | CO2是導致酸雨發生的主要原因 | |
| C. | 可用Na2CO3溶液捕捉(吸收)CO2 | |
| D. | 使用氫能源替代化石燃料可減少CO2排放 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下氯氣與燒堿溶液反應:Cl2+2OH-═Cl-+ClO-+H2O | |
| B. | AlCl3溶液中加入過量的氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| C. | 金屬鈉與水反應:Na+H2O═Na++OH-+H2↑ | |
| D. | 銅與稀硝酸反應:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 振蕩分液漏斗時應關閉其玻璃塞和活塞 | |
| B. | 用濕潤的碘化鉀淀粉試紙鑒別Br2(g)和NO2 | |
| C. | 在50mL量筒中配制0.1000mol•L-1碳酸鈉溶液 | |
| D. | 檢驗NH4+時,向試樣中加入NaOH溶液,微熱,用濕潤的藍色石蕊試紙檢驗逸出的氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 正反應是吸熱反應,且A不是氣態 | B. | 正反應是放熱反應,且A不是氣態 | ||
| C. | 正反應是吸熱反應,且A是氣態 | D. | 正反應是放反應,且A是氣態 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
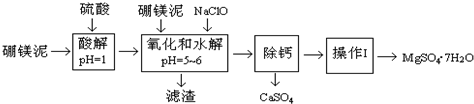
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 |
| 開始沉淀pH | 2.3 | 4.0 | 7.6 |
| 完全沉淀pH | 4.1 | 5.2 | 9.6 |
| 溫度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題


查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 氫氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
| Ksp | 8.0×10-16 | 1.0×10-29 | 1.8×10-11 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 )的廢水可以通過構成微生物電池除去,其原理如圖所示.
)的廢水可以通過構成微生物電池除去,其原理如圖所示.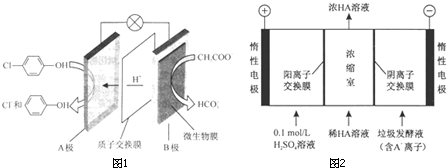
 -OH+2e-+H+═
-OH+2e-+H+═ -OH+Cl-.
-OH+Cl-.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com