
| 元素 | 相關信息 |
| A | 原子核外L層電子數是K層的2倍 |
| B | 其一種單質被稱為地球生物的“保護傘” |
| C | 元素的第一電離能是第3周期所有元素中最小的 |
| D | 基態原子最外層電子排布為(n+1)sn(n+1)p(n+2) |
| E | 可形成多種氧化物,其中一種為具有磁性的黑色晶體 |
分析 A元素原子核外L層電子數是K層的2倍,則L層有4個電子,故A為碳元素;B元素的一種單質被稱為地球生物的“保護傘”,故B為氧元素;C元素的第一電離能是第3周期所有元素中最小的,故C為Na元素;D元素基態原子最外層電子排布為(n+1)sn(n+1)p(n+2),由于n=2,故D為S元素;E元素可形成多種氧化物,其中一種為具有磁性的黑色晶體,故E為Fe元素,據此解答.
解答 解:A元素原子核外L層電子數是K層的2倍,則L層有4個電子,故A為碳元素;B元素的一種單質被稱為地球生物的“保護傘”,故B為氧元素;C元素的第一電離能是第3周期所有元素中最小的,故C為Na元素;D元素基態原子最外層電子排布為(n+1)sn(n+1)p(n+2),由于n=2,故D為S元素;E元素可形成多種氧化物,其中一種為具有磁性的黑色晶體,故E為Fe元素.
(1)C為Na元素,處于周期表中第三周期IA族,D為硫元素,基態原子核外電子排布式是1s22s22p63s23p4,
故答案為:三、IA;1s22s22p63s23p4;
(2)B、C、D的簡單離子分別為O2-、Na+、S2-,電子層排布相同,核電荷數越大離子半徑越小,最外層電子數相同,電子層越多離子半徑越大,故離子半徑由大到小的順序為:S2->O2->Na+,
由于非金屬性O>S,故氣態氫化物中穩定性H2O>H2S,
故答案為:S2->O2->Na+;H2O;
(3)B、C的單質按物質的量比1:2形成的化合物為Na2O2,含有離子鍵、共價鍵,屬于離子晶體,
故答案為:離子鍵、共價鍵;離子;
(4)E的黑色磁性晶體為Fe3O4,發生鋁熱反應的化學方程式是:3Fe3O4+8Al$\frac{\underline{\;高溫\;}}{\;}$9Fe+4Al2O3,
故答案為:3Fe3O4+8Al$\frac{\underline{\;高溫\;}}{\;}$9Fe+4Al2O3.
點評 本題考查結構性質位置關系、核外電子排布規律、微粒半徑比較、化學鍵等,難度不大,旨在考查學生對基礎知識的全面掌握.


科目:高中化學 來源: 題型:選擇題
| A. | 加H2O | B. | 加入飽和食鹽水 | ||
| C. | 增大壓強 | D. | 升高溫度(不考慮鹽酸揮發) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Mg | B. | $\frac{1}{M}$g | C. | $\frac{M}{6.02×1{0}^{23}}$g | D. | $\frac{6.02×1{0}^{23}}{\;}$g |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 ,M的化學式為FeS,F的電子式為
,M的化學式為FeS,F的電子式為 .
. .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 冰醋酸、純堿、芒硝、生石灰分別屬于酸、堿、鹽、氧化物 | |
| B. | HClO、H2SO4(濃)、HNO3均具有強氧化性,都是氧化性酸 | |
| C. | 漂白粉、福爾馬林、冰水、王水、氯水均為混合物 | |
| D. | Na2O,NaOH,Na2CO3,NaCl,Na2SO4,Na2O2都屬于鈉的含氧化合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
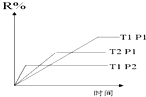
| A. | 正反應吸熱,L是氣體 | B. | 正反應吸熱,L是固體 | ||
| C. | 正反應放熱,L是氣體 | D. | 正反應放熱,L是固體 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 氧化亞銅(Cu2O)作為一種重要的無機化工原料,在涂料、有色玻璃和催化劑等領域有著廣泛的用途.回答下列問題:
氧化亞銅(Cu2O)作為一種重要的無機化工原料,在涂料、有色玻璃和催化劑等領域有著廣泛的用途.回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | C2H4、C2H2 | B. | CH4、C2H6 | C. | CH4、C2H4 | D. | C2H2、C3H6 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 向100mLBaCl2、AlCl3、FeCl3 的混合溶液A中逐滴加入Na2SO4和NaOH的混合溶液B,產生沉淀的物質的量n和加入溶液B的體積關系如圖所示:
向100mLBaCl2、AlCl3、FeCl3 的混合溶液A中逐滴加入Na2SO4和NaOH的混合溶液B,產生沉淀的物質的量n和加入溶液B的體積關系如圖所示:| 溶質 | Na2SO4 | NaOH | BaCl2 | AlCl3 | FeCl3 |
| c/mol•L-1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com