
| A. | 鋁與Fe2O3發生鋁熱反應后固體物質增重 | |
| B. | Al片溶于NaOH溶液,產生氣體:2Al+2OH-+2H2O═2AlO2-+3H2↑ | |
| C. | 工業上電解熔融狀態的Al2O3制備Al | |
| D. | 鋁制容器可盛裝濃H2SO4 |
分析 A、Fe2O3與Al粉混合物發生鋁熱反應,實質是置換反應,生成鐵和氧化鋁,由此分析解答;
B、Al片溶于NaOH溶液,反應生成偏鋁酸鈉和氫氣,反應的離子方程式為:2Al+2OH-+2H2O═2AlO2-+3H2↑;
C、電解熔融狀態的Al2O3得到Al和氧氣;
D、鋁與冷的濃硫酸發生鈍化現象.
解答 解:A、Fe2O3與Al粉混合物發生鋁熱反應,實質是置換反應,生成鐵和氧化鋁,方程式為:2Al+Fe2O3═2Fe+Al2O3,鐵的相對原子質量為56,而鋁的相對原子質量為27,所以固體質量減輕,故A錯誤;
B、Al片溶于NaOH溶液,反應生成偏鋁酸鈉和氫氣,反應的離子方程式為:2Al+2OH-+2H2O═2AlO2-+3H2↑,故B正確;
C、電解熔融狀態的Al2O3得到Al和氧氣,工業上用此方法制得鋁,故C正確;
D、鋁與冷的濃硫酸發生鈍化現象,所以鋁制容器可盛裝濃H2SO4,故D正確;
故選A.
點評 本題考查鋁的制備和鋁的化學性質,鋁與氫氧化鈉反應的離子方程式中水是氧化劑,書寫過程中不能漏掉水,比較容易.


科目:高中化學 來源: 題型:選擇題
| A. | 苯分子中C原子均以sp3雜化方式成鍵,形成夾角為120°的三個sp3雜化軌道,故為正六邊形的碳環 | |
| B. | 每個碳原子還有一個未參與雜化的2p軌道,垂直碳環平面,相互交蓋,形成大π鍵 | |
| C. | 大π鍵中6個電子被6個C原子共用,故稱為6中心6電子大π鍵 | |
| D. | 苯分子中共有十二個原子共面,六個碳碳鍵完全相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氫氧化鋇溶液與稀硫酸的反應:OH-+H++Ba2++SO42-=BaSO4↓+H2O | |
| B. | 硫酸鋁溶液中加入過量氨水:Al3++4OH-═[Al(OH)4]- | |
| C. | 用FeCl3溶液腐蝕銅線路板:Cu+2Fe3+=Cu2++2Fe2+ | |
| D. | 碳酸鈣溶于稀鹽酸中:CO32-+2H+=H2O+CO2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 苯、乙醇和乙酸都能發生取代反應 | |
| B. | 液化石油氣和天然氣的主要成分都是甲烷 | |
| C. | 油脂在堿的催化作用下可發生水解,工業上利用該反應生產肥皂 | |
| D. | 用新制的Cu(OH)2懸濁液可檢驗尿液中的葡萄糖 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1 000mL | B. | 500mL | C. | 100mL | D. | 1 500mL |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | c(H+)=c(CH3COO-)+c(OH-) | B. | c (Na+)>c (CH3COO-)>c(OH-)>c(H+) | ||
| C. | c(Na+)=c(CH3COO-)>c(OH-)=c(H+) | D. | c (CH3COO-)>c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 煤的氣化就是將煤在高溫條件由固態轉化為氣態的物理變化過程 | |
| B. | 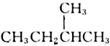 和 和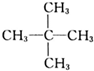 互為同分異構體 互為同分異構體 | |
| C. | 淀粉、蛋白質和油脂都是高聚物,在一定條件下都能水解 | |
| D. | 石油裂解可以得到更多的汽油,這種汽油是一種純凈物 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com