
| A. | 用pH試紙測定Na2CO3溶液的pH | |
| B. | 從食鹽水中提取NaCl | |
| C. | 用新制的FeSO4溶液和NaOH溶液制備Fe(OH)2 | |
| D. | 配制100ml 0.1000mol/L的NaCl溶液 |
分析 A.用pH試紙測定Na2CO3溶液的pH,可用玻璃棒蘸取溶液;
B.從食鹽水中提取NaCl,用到過濾和蒸發操作;
C.無需使用玻璃棒;
D.配制一定物質的量濃度的溶液用玻璃棒攪拌和引流.
解答 解:A.用pH試紙溶液的pH,可用玻璃棒蘸取溶液,滴在玻璃片上的pH試紙上觀察,故A正確;
B.從食鹽水中提取NaCl,用到過濾和蒸發操作,分別用玻璃棒進行引流和攪拌,故B正確;
C.用新制的FeSO4溶液和NaOH溶液制備Fe(OH)2不需要使用玻璃棒,故C錯誤;
D.配制一定物質的量濃度的氯化鈉溶液用玻璃棒攪拌和引流,故D正確.
故選C.
點評 本題考查化學實驗基本操作,題目難度不大,注意常見化學基本操作以及實驗的注意事項.


科目:高中化學 來源: 題型:選擇題
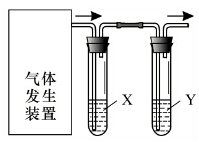 實驗室用如圖裝置完成下表所列的四個實驗,不能達到實驗目的是( )
實驗室用如圖裝置完成下表所列的四個實驗,不能達到實驗目的是( ) | 選項 | 實驗目的 | 試劑X | 試劑Y |
| A | 驗證C2H5OH與濃H2SO4加熱至170℃制得的乙烯的性質 | NaOH溶液 | Br2水 |
| B | 檢驗FeSO4受熱分解產生的氣體中由SO3和SO2 | BaCl2溶液 | 品紅溶液 |
| C | 驗證電石與飽和食鹽水反應生成的乙炔的性質 | CuSO4溶液 | KMnO4溶液 |
| D | 驗證氧化性:Cl2>Br2>I2 | NaBr溶液 | KI溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
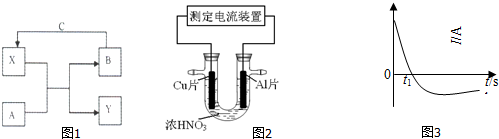
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗編號 | HA物質的量濃度 (mol•L-1) | NaOH物質的量濃度 (mol•L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | C1 | 0.2 | pH=7 |
| 丙 | 0.1 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=10 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 滴定次數 | 待測溶液的體積/mL | 標準溶液的體積/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2KMnO4+16HCl(濃)═2KCl+2MnCl2+5Cl2↑+8H2O | |
| B. | 2HCl$\frac{\underline{\;通電\;}}{\;}$H2↑+Cl2↑ | |
| C. | HCl+AgNO3═AgCl↓+HNO3 | |
| D. | Zn+2HCl═ZnCl2+H2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 甲烷的標準燃燒熱為-890.3 kJ•molˉ1,則甲烷燃燒的熱化學方程式可表示為CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•molˉ1 | |
| B. | 由C(石墨,s)=C(金剛石,s)△H=+1.9 kJ•molˉ1可知,金剛石比石墨穩定 | |
| C. | 在稀溶液中:H+(aq)+OHˉ(aq)=H2O(l)△H=-57.3 kJ•molˉ1,若將含1 mol CH3COOH與含1 mol NaOH的溶液混合,放出的熱量小于57.3 kJ | |
| D. | 一定條件下,某密閉容器中充入2 mol SO2(g)和1 mol O2(g),達到平衡后,放出Q kJ熱量,則該條件下的熱化學方程式為:2SO2(g)+O2(g)?2SO3(g )△H=-Q kJ•molˉ1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com