
| 實驗組 | 溫度/℃ | 起始量/mol | 平衡量/mol | 達到平衡所需要的時間/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
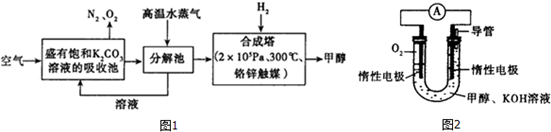
分析 (1)KHCO3受熱易分解;
(2)依據熱化學方程式和蓋斯定律計算得到;
(3)甲醇燃燒的反應原理,設計如圖所示的電池裝置,甲醇在負極失電子發生氧化反應,正極是氧氣得到電子生成氫氧根離子,依據原電池原理分析書寫電極反應;
(4)Na2CO3溶液的濃度為0.02mol/L,等體積混合后溶液中c(CO32-)=0.01mol/L,根據Ksp=c(CO32-)•c(Ca2+)計算沉淀時混合溶液中c(Ca2+),原溶液CaCl2溶液的最小濃度為混合溶液中c(Ca2+)的2倍;
(5)①根據v=$\frac{△c}{△t}$計算反應速率;
②根據平衡常數表達式計算出實驗2的平衡常數;
③根據溫度變化,平衡時的生成物的物質的量的多少判斷平衡移動的方向,判斷反應熱的符號;
解答 解:(1)KHCO3受熱易分解,向分解池中通入高溫水蒸氣,提供高溫環境使KHCO3分解,
故答案為:提供高溫環境使KHCO3分解;
(2)①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1275.6kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ/mol
③H2O(g)=H2O(l)△H=-44.0kJ/mol
依據蓋斯定律①-②+③×4得到甲醇不完全燃燒生成一氧化碳和液態水的熱化學方程式:2CH3OH(l)+2O2(g)=2CO (g)+4H2O(l)△H=-885.6KJ/mol,
得到熱化學方程式為:CH3OH(l)+O2(g)=CO (g)+2H2O(l)△H=-442.8KJ/mol,
故答案為:CH3OH(l)+O2(g)=CO (g)+2H2O(l)△H=-442.8KJ/mol;
(3)甲醇燃燒的反應原理,設計如圖所示的電池裝置,甲醇在負極失電子發生氧化反應,CH3OH+8OH--6e-=CO32-+6H2O,
故答案為:CH3OH+8OH--6e-=CO32-+6H2O;
(4)Na2CO3溶液的濃度為0.02mol/L,等體積混合后溶液中c(CO32-)=$\frac{1}{2}$×0.02mol/L=0.01mol/L,根據Ksp=c(CO32-)•c(Ca2+)=2.8×10-9可知,c(Ca2+)=$\frac{2.8×1{0}^{-9}}{0.01}$mol/L=2.8×10-7mol/L,原溶液CaCl2溶液的最小濃度為混合溶液中c(Ca2+)的2倍,故原溶液CaCl2溶液的最小濃度為2×2.8×10-7mol/L=5.6×10-7mol/L,
故答案為:5.6×10-7mol/L;
(5)①v(CO2)=v(CO)=$\frac{4mol-2.4mol}{2L×6min}$=0.13 mol/(L.min),故答案為:0.13 mol/(L.min);
②實驗2中達到平衡時,c(CO2)=c(H2)=$\frac{0.4mol}{2L}$=0.2mol/L,c(CO)=$\frac{1.6mol}{2L}$=0.8mol/L,c(H2O)=$\frac{1mol-0.4mol}{2L}$=0.3mol/L,
K=$\frac{0.2×0.2}{0.8×0.3}$≈0.17,
故答案為:0.17;
③根據CO(g)+H2O(g)?CO2(g)+H2(g)可知壓強對平衡移動無影響,如果在650℃,H2O、CO的物質的量改為1mol、2mol,達到平衡時CO的物質的量應為1.2mol,而900℃時CO的物質的量應為1.6mol,說明升高溫度平衡向逆反應方向移動,則正反應為放熱反應,即△H<0,
故答案為:<;
點評 本題考查了蓋斯定律的應用、原電池原理、反應速率的計算、平衡常數的計算與運用、溶度積的有關計算等,題目綜合性較強,是對學生能力的考查,難度中等,注意把握反應原理的有關內容.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
 過氧化氫(H2O2)被稱為綠色氧化劑,其分子結構如圖所示.兩個氫原子位于不重合的兩個平面上,而兩個氧原子位于兩平面的交線上.下列有關說法正確的是( )
過氧化氫(H2O2)被稱為綠色氧化劑,其分子結構如圖所示.兩個氫原子位于不重合的兩個平面上,而兩個氧原子位于兩平面的交線上.下列有關說法正確的是( )| A. | 過氧化氫分子中含有H-H鍵、O-O鍵 | |
| B. | 過氧化氫分子中存在離子鍵和共價鍵 | |
| C. | 過氧化氫分子中只有共價鍵,其電子式為 | |
| D. | H2O2與H2O互為同位素 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 酸與醇反應一定能生成酯,且酯化反應是可逆反應 | |
| B. | CO2通入飽和苯酚鈉溶液,用分液法可以得到苯酚 | |
| C. | 有機物 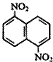 的n溴代物的同分異構體的數目與m溴代物的同分異構體的數目相等,則m、n一定滿足的關系式m+n=6 的n溴代物的同分異構體的數目與m溴代物的同分異構體的數目相等,則m、n一定滿足的關系式m+n=6 | |
| D. | 等物質的量的烴或烴的含氧衍生物A和B完全燃燒時,消耗氧氣的量相等.則A和B的分子量相差可能為18n或44n(n為正整數) |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
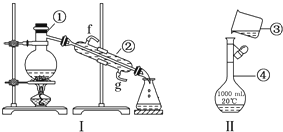
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始濃度(mol/L) | 2.0 | 1.0 | 0 |
| 平衡濃度(mol/L) | c1 | c2 | 0.4 |
| A. | 10 min內,v(Cl2)=0.04 mol/(L•min) | |
| B. | 當容器中Cl2為1.2 mol時,反應達到平衡 | |
| C. | 升高溫度(T1<T2),反應的平衡常數減小,平衡時PCl3的$\frac{△n({T}_{1})}{△n({T}_{2})}$<1 | |
| D. | 平衡后移走2.0 mol PCl3和1.0 molCl2,在相同條件下再達平衡時,c(PCl5)<0.2 mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 水比硫化氫氣體穩定 | B. | 水的熔沸點比硫化氫高 | ||
| C. | 氯化氫氣體易溶于水 | D. | 過氧化氫易分解 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氧化鎳高溫分解 | B. | 電解熔融的氧化鎳 | ||
| C. | 高溫下用氫氣還原氧化鎳 | D. | 高溫下用焦炭還原氧化鎳 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com