
原電池正、負電極的極性不僅與電極材料的性質有關,也與電解質溶液有關。下列由不同材料組成的原電池,電極反應正確的是
A.由Fe、Cu與稀硫酸組成的原電池,其負極反應式為Fe-3e-=Fe3+
B.由Al、Mg與氫氧化鈉溶液組成的原電池,其負極反應式為:Mg-2e-+2OH-=Mg(OH)2
C.Pb、Cu與氯化鐵溶液組成的原電池,其正極反應式為Cu-2e-=Cu2+
D.Al、Cu與濃硝酸組成的原電池,其負極反應式為Cu-2e-=Cu2+
D
【解析】
試題分析:原電池中較活潑的金屬做負極,不活潑的金屬做正極,但在實際判斷時還需要考慮電解質溶液的性質。A、由Fe、Cu與稀硫酸組成的原電池中鐵的金屬性強于銅,且鐵能和稀硫酸反應,因此其負極是鐵,則負極反應式為Fe-2e-=Fe2+,A不正確;B、由Al、Mg與氫氧化鈉溶液組成的原電池,鎂的金屬性強于鋁,但能和氫氧化鈉溶液反應的是鋁,因此鋁是負極,鎂是正極,則負極反應式為Al-3e-+4OH-=AlO2-+2H2O,B不正確;C、Pb、Cu與氯化鐵溶液組成的原電池中銅的金屬性強于鉛,因此銅是負極,鉛是正極,則正極反應式為Fe3+-2e-=Fe2+,C不正確;D、Al、Cu與濃硝酸組成的原電池中鋁比銅活潑,但常溫下鋁在濃硝酸中鈍化,因此鋁是正極,銅是負極,其負極反應式為Cu-2e-=Cu2+,D正確,答案選D。
考點:考查原電池正負極以及電極反應式的書寫判斷


 開心蛙口算題卡系列答案
開心蛙口算題卡系列答案科目:高中化學 來源: 題型:
 原電池是化學對人類的一項重大貢獻.
原電池是化學對人類的一項重大貢獻.查看答案和解析>>
科目:高中化學 來源:2012-2013學年陜西省長安一中高一下學期期中考試化學試卷(帶解析) 題型:填空題
有如下兩個反應:
A 2HCl+Ba(OH)2===BaCl2+2H2O
B 2Fe3++Cu==2Fe2++Cu2+
(1) 根據兩反應的本質,判斷能否設計成原電池:A B (填“能”或“不能” )不能設計成原電池的原因是
(2) 根據能設計成原電池的反應選擇適合的材料和試劑設計一個原電池
①負極材料是_______,正極材料是________,電解質溶液是 ___;
②寫出負極的電極反應式 _;
③原電池工作時溶液中的Cl-從__________極向________極移動(填正或負)
④若導線上轉移電子0.2mol,則負極質量變化是 ___ 減少 ___ ; 將此反應設計成原電池,若電解質溶液為H2SO4,
將此反應設計成原電池,若電解質溶液為H2SO4,
請寫出正負極的電極反應;負極:_______________;正極:______________。
查看答案和解析>>
科目:高中化學 來源:2011-2012學年北京市朝陽區高一下學期期末統一考試化學試卷(帶解析) 題型:實驗題
(10分)原電池是化學對人類的一項重大貢獻。
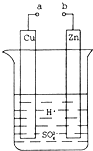
(1)某興趣小組為研究原電池原理,設計如圖裝置。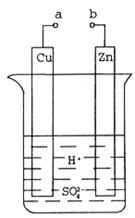
①a和b不連接時,燒杯中發生反應的離子方程式是__________。
②a和b用導線連接,Cu極為原電池__________極(填“正”或“負”),電極反應式是__________。Zn極發生__________(填“氧化”或“還原”)反應。溶液中H+移向__________(填“Cu”或“Zn”)極。
③無論a和b是否連接,Zn片均被腐蝕。若轉移了0.2mol電子,則理論上Zn片質量減輕了__________g。
(2)有同學想把Ba(OH)2?8H2O晶體與NH4Cl晶體的反應設計成原電池,你認為是否可行?________(填“是”或“否”),理由是__________。
查看答案和解析>>
科目:高中化學 來源:2015屆陜西省高一下學期期中考試化學試卷(解析版) 題型:填空題
有如下兩個反應:
A 2HCl+Ba(OH)2===BaCl2+2H2O
B 2Fe3++Cu==2Fe2++Cu2+
(1) 根據兩反應的本質,判斷能否設計成原電池:A B (填“能”或“不能” )不能設計成原電池的原因是
(2) 根據能設計成原電池的反應選擇適合的材料和試劑設計一個原電池
①負極材料是_______,正極材料是________,電解質溶液是 ___;
②寫出負極的電極反應式 _;
③原電池工作時溶液中的Cl-從__________極向________極移動(填正或負)
④若導線上轉移電子0.2mol,則負極質量變化是 ___ 減少 ___ ;
 將此反應設計成原電池,若電解質溶液為H2SO4,
將此反應設計成原電池,若電解質溶液為H2SO4,
請寫出正負極的電極反應;負極:_______________;正極:______________。
查看答案和解析>>
科目:高中化學 來源:2014屆北京市朝陽區高一下學期期末統一考試化學試卷(解析版) 題型:實驗題
(10分)原電池是化學對人類的一項重大貢獻。
(1)某興趣小組為研究原電池原理,設計如圖裝置。
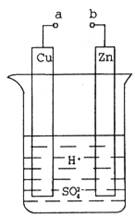
①a和b不連接時,燒杯中發生反應的離子方程式是__________。
②a和b用導線連接,Cu極為原電池__________極(填“正”或“負”),電極反應式是__________。Zn極發生__________(填“氧化”或“還原”)反應。溶液中H+移向__________(填“Cu”或“Zn”)極。
③無論a和b是否連接,Zn片均被腐蝕。若轉移了0.2mol電子,則理論上Zn片質量減輕了__________g。
(2)有同學想把Ba(OH)2•8H2O晶體與NH4Cl晶體的反應設計成原電池,你認為是否可行?________(填“是”或“否”),理由是__________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com