
下列有關物質用途的說法中,正確的是( )
A.二氧化硅可用作半導體材料
B.硝酸常用作金屬銅加工前的酸洗
C.碳酸鈉可用于治療胃酸過多
D.三氧化二鐵常用于生產紅色油漆和涂料
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
能源可劃分為一級能源和二級能源。自然界中以現成的形式提供的能源被稱為一級能源,需依靠其他能源的能量間接制取的能源被稱為二級能源。下列敘述不正確的是 ( )
A、電能是二級能源 B、水力是二級能源
C、天然氣是一級能源 D、木柴是一級能源
查看答案和解析>>
科目:高中化學 來源: 題型:
下列有關實驗裝置的說法中正確的是( )

A.用圖1裝置制取干燥純凈的NH3
B.用圖2裝置實驗室制備Fe(OH)2
C.用圖3裝置可以完成“噴泉”實驗
D.用圖4裝置測量Cu與濃硝酸反應產生氣體的體積
查看答案和解析>>
科目:高中化學 來源: 題型:
下列有關物質性質和用途的說法,正確的是( )
A.光導纖維具有很強的導電能力,所以大量用于制造通信光纜
B.明礬常用作凈水劑,是因為它具有消毒殺菌的作用
C.氨常用作制冷劑,是因為其沸點極低,很容易液化
D.SiCl4在戰爭中常用作煙霧彈,是因為它與水反應時生成白色煙霧
查看答案和解析>>
科目:高中化學 來源: 題型:
用如圖所示裝置進行實驗,下列對實驗現象的解釋不合理的是( )
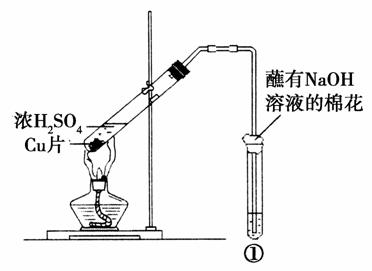
| 選項 | ①中試劑 | ①中現象 | 解釋 |
| A | Ba(NO3)2溶液 | 生成白色沉淀 | SO |
| B | 品紅溶液 | 溶液褪色 | SO2具有漂白性 |
| C | 紫色石蕊溶液 | 溶液變紅 | SO2與水反應生成酸 |
| D | 酸性KMnO4溶液 | 紫色褪去 | SO2具有還原性 |
查看答案和解析>>
科目:高中化學 來源: 題型:
鹵素單質的性質活潑,鹵素的化合物應用廣泛,運用化學反應原理研究鹵族元素的有關性質具有重要意義。
(1)下列關于氯水的敘述正確的是________(填寫序號)。
A.氯水中存在兩種電離平衡
B.向氯水中通入SO2,其漂白性增強
C.向氯水中通入氯氣,c(H+)/c(ClO-)減小
D.加水稀釋氯水,溶液中的所有離子濃度均減小
E.加水稀釋氯水,水的電離平衡向正反應方向移動
F.向氯水中加少量固體NaOH,可能有c(Na+)=c(Cl-)+c(ClO-)
(2)工業上通過氯堿工業生產氯氣,其反應的離子方程式為____。
(3)常溫下,已知25 ℃時有關弱酸的電離平衡常數:
| 弱酸化學式 | HClO | H2CO3 |
| 電離平衡常數 | K=3.0×10-8 | K1=4.4×10-7,K2=4.7×10-11 |
寫出84消毒液(主要成分為NaClO)露置在空氣中發生反應的有關化學方程式________________________。若將84消毒液與潔廁劑(含有濃鹽酸)混合使用可能會導致中毒,請用離子方程式解釋有關原因__________________。
(4)碘鎢燈具有比白熾燈壽命長且環保節能的特點。一定溫度下,燈內封存的少量碘與使用過程中沉積在管壁上的鎢可以發生反應:W(s)+I2(g)WI2(g)。為模擬上述反應,準確稱取0.508 g碘、0.736 g金屬鎢置于50.0 mL的密閉容器中,加熱使其反應。
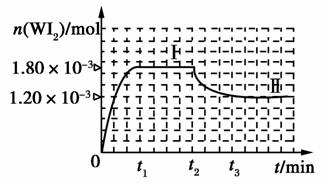
如圖是WI2(g)的物質的量隨時間變化的關系圖像,其中曲線I(0~t2時間段)的反應溫度為T1,曲線Ⅱ(從t2開始)的反應溫度為T2,且T2>T1。則:
①該反應的ΔH________0(填“>”、“=”或“<”)。
②從反應開始到t1時間內的平均反應速率v(I2)=________。
③下列說法中不正確的是________(填序號)。
A.利用該反應原理可以提純鎢
B.該反應的平衡常數表達式是K=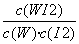
C.燈絲附近溫度越高,燈絲附近區域WI2越易變為W而重新沉積到燈絲上
(5)25 ℃時,向5 mL含有KCl和KI濃度均為0.1 mol·L-1的混合液中,滴加6 mL 0.1 mol·L-1的AgNO3溶液,先生成的沉淀是________,溶液中離子濃度由大到小的順序是________[不考慮H+和OH-。25 ℃時Ksp(AgCl)=1.8×10-10、Ksp(AgI)=8.3×10-17]。
查看答案和解析>>
科目:高中化學 來源: 題型:
下列實驗現象中,由于發生取代反應而引起的是( )
A.乙烯通入溴的四氯化碳溶液中,溶液褪色
B.甲烷和氯氣的混合氣體在光照后,瓶壁上有油狀液滴附著
C.苯滴加到溴水中,振蕩后水層接近無色
D.將灼熱的銅絲迅速插入乙醇中,反復多次,有刺激性氣味產生
查看答案和解析>>
科目:高中化學 來源: 題型:
某市對大氣進行監測,發現該市首要污染物為可吸入顆粒物PM2.5(直徑小于等于2.5μm的懸浮顆粒物),其主要來源為燃煤、機動車尾氣等。因此,對PM2.5、SO2、NOx等進行研究具有重要意義。
請回答下列問題:
(1)將PM2.5樣本用蒸餾水處理制成待測試樣。
若測得該試樣所含水溶性無機離子的化學組分及其平均濃度如下表:
| 離子 | K+ | Na+ | N | S | N | Cl- |
| 濃度/mol·L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
根據表中數據判斷PM2.5的酸堿性為 ,試樣的pH= 。
(2)為減少SO2的排放,常采取的措施有:
①將煤轉化為清潔氣體燃料。
已知:H2(g)+ O2(g)
O2(g) H2O(g) ΔH=-241.8 kJ·mol-1
H2O(g) ΔH=-241.8 kJ·mol-1
C(s)+ O2(g)
O2(g) CO(g) ΔH=-110.5 kJ·mol-1
CO(g) ΔH=-110.5 kJ·mol-1
寫出焦炭與水蒸氣反應的熱化學方程式: 。
②洗滌含SO2的煙氣。以下物質可作洗滌劑的是 。
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(3)汽車尾氣中NOx和CO的生成及轉化
①已知汽缸中生成NO的反應為:
N2(g)+O2(g) 2NO(g) ΔH>0
2NO(g) ΔH>0
若1 mol空氣含0.8 mol N2和0.2 mol O2,1 300℃時在密閉容器內反應達到平衡,測得NO為8×10-4mol。計算該溫度下的平衡常數K= 。
汽車啟動后,汽缸溫度越高,單位時間內NO排放量越大,原因是 。
②汽車燃油不完全燃燒時產生CO,有人設想按下列反應除去CO:
2CO(g) 2C(s)+O2(g)
2C(s)+O2(g)
已知該反應的ΔH>0,簡述該設想能否實現的依據:
。
③目前,在汽車尾氣系統中裝置催化轉化器可減少CO和NO的污染,其化學反應方程式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:
下表中對應關系正確的是
| A | CH3CH3+Cl2 CH2=CH2+HCl | 均為取代反應 |
| B | 由油脂得到甘油 由淀粉得 | 均發生了水解反應 |
| C | Cl2+2Br‾=2Cl‾+Br2 Zn+Cu2+=Zn2++Cu | 均為單質被還原的置換反應 |
| D | 2Na2O2+2H2O+4NaOH+O2↑ Cl2+H2O=HCl+HClO | 均為水作還原劑的氧化還原反應 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com