
下表給出了五種元素的相關信息,其中w、X、Y、Z為短周期元素,原子序數(shù)依次遞增。
| 元素 | 相關信息 |
| W | 單質為密度最小的氣體 |
| X | 元素最高正價與最低負價之和為0 |
| Y | 工業(yè)上通過分離液態(tài)空氣獲得其單質,該單質的某種同素異形體是保護地球地表環(huán)境的重要屏障 |
| Z | 存在質量數(shù)為23,中子數(shù)為12的核素 |
| T | 金屬單質為紅色,導電性好,是人體不可缺少的徽量元素,焰色反應時火焰為綠色 |
(10分)
(1)第二周期 第ⅥA族(2分);范德華力(1分)
(2)Na2O2(2分)
(3)2C2H2(g)+5O2(g) =4CO2(g)+2H2O(g) △H=—26QkJ/mol(3分)
(4)Cu2(OH)2CO3=2CuO+CO2+H2O(2分)
解析試題分析:W單質為密度最小的氣體,W為氫;X為第ⅣA族元素,結合前后信息,只能是碳元素;Y為氧元素;Z的質子數(shù)為11,Z為鈉元素;根據(jù)單質顏色和焰色,T為銅元素。
(1)氧元素位于元素周期表第二周期ⅥA族;CO2是分子晶體,從固態(tài)到氣態(tài)需克服分子間作用力(范德華力)。
(2)由鈉和氧組成的強氧化劑是Na2O2
(3)含極性共價鍵和非極性共價鍵的相對分子質量最小的分子為乙炔,2g乙炔反應放出放熱QkJ ,則2mol乙炔(52g)燃燒放出26QkJ ,可得2C2H2(g)+5O2(g) =4CO2(g)+2H2O(g) △H=—26QkJ/mol。
(4)化合物丙僅由W、X、Y、Z、T中的四種元素組成,四種元素的質量比為1:6:40:64,64必為銅;而40的整數(shù)倍可能是只有氧的原子量倍數(shù),可以有5個氧原子,依次推出1個碳,2個氫,結合題意為Cu2(OH)2CO3,
考點:本題以元素推斷為基礎,考查物質結構、元素周期律、元素及化合物、熱化學方程式的書寫等知識。


科目:高中化學 來源: 題型:填空題
甲、乙、丙、丁、戊五種短周期元素原子序數(shù)依次遞增。甲最外層電子數(shù)是次外層的兩倍,丙的次外層電子數(shù)比最外層少4個,丁形成的簡單陽離子是同周期元素簡單離子中半徑最小的,戊是同周期主族元素中原子半徑最小的。試用化學式回答下列問題:
(1)乙和戊形成的化合物中各原子最外層均滿足8e-結構,其化學式為 ;
(2)寫出乙的最高價氧化物的水化物的濃溶液與甲單質反應的化學方程式 ;
(3)戊的最高價氧化物與丁的最高價氧化物的水化物反應的離子反應方程式為 ;
(4)常溫下戊單質被NaOH溶液吸收的化學方程式為 ;
(5)氫與丙形成原子個數(shù)比為1:1的液體,該物質中存在的作用力有( )
①極性鍵 ②非極性鍵 ③離子鍵 ④氫鍵 ⑤范德華力
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
短周期元素X、Y、Z、W原子序數(shù)依次增大。X氫化物的水溶液顯堿性;Y在元素周期表中所處的周期序數(shù)與族序數(shù)相等;Z單質是將太陽能轉化為電能的常用材料;W是重要的“成鹽元素”,主要以鈉鹽的形式存在于海水中。請回答:
(l)Y在元素周期表中的位置是__________;X氫化物的電子式是__________。
(2)X氫化物的水溶液與W氫化物的水溶液混合后恰好反應時,溶液呈__________(填“酸”、“堿”或“中”)性,用離子方程式表示其原因是__________。
(3)Y-AgO電池是應用廣泛的魚雷電池,其原理如下圖所示。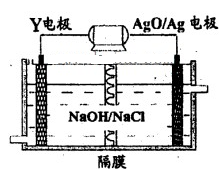
該電池的負極反應式是__________。
(4)Z和W比較,非金屬性較弱的是__________(填元素符號),下列可以驗證這一結論的是__________(填序號)。
a.元素在地殼中的含量
b.最高價氧化物對應水化物的酸性
c.斷開氫化物中1molH-Z或H-W鍵所需的能量
d.Z與W以共價鍵形成化合物時,Z或W顯示的電性
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、D、E五種短周期元素,原子序數(shù)依次增大,A原子的最外層電子排布式為nsnnpn+1,C、D原子核外都有一個未成對電子,又知B和E為同一主族,C、D、E為同周期,且B、E的原子序數(shù)之和等于C、D的原子序數(shù)之和
(1) E離子的基態(tài)電子排布式 _______________
(2)元素B、C、D、E的原子半徑從大到小的順序是________(用元素符號填寫,下同)
(3)元素A、B、C、D的第一電離能從大到小的順序是
(4)寫出C單質與B單質加熱時生成的化合物的電子式
(5) D元素在周期表中的位置是_______________,中學化學實驗室中制取D的最高價氧化物對應的水化物的離子方程式為___________________________________
(6)已知:①A2(g)+B2(g)=2AB(g) ΔH1=akJ/mol
②2AB(g)+B2(g)=2AB2(g) ΔH2=bkJ/mol
③AB(g)+AB2(g)= A2B3(g) ΔH3=ckJ/mol
則2A2(g)+3B2(g)=2A2B3(g) ΔH= kJ/mol (用a.b.c表示)
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、D是元素周期表前四周期常見的四種元素,原子序數(shù)依次增大, 它們的相關結構和性質信息如下表所示,請結合相關信息,完成相關的問題:
| 元素 | 相關結構和性質 |
| A | A為非金屬元素,其一種單質是電的良導體,難熔、質軟并有潤滑性,可用作電極材料 |
| B | 是蛋白質的組成元素之一,原子核外有三種不同能量的電子,且未成對電子數(shù)最多 |
| C | 其單質既能與強酸溶液應又能與強堿溶液反應,其簡單離子在第三周期單核離子中半徑最小 |
| D | D的高價氯化物的鹽溶液常用于印刷電路極電路的“刻蝕” |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
現(xiàn)有五種短周期主族元素A、B、C、 D、E,其原子序數(shù)依次增大。A原子約占宇宙中原子總數(shù)的88.6%,A+又稱為質子:B是形成化合物種類最多的元素,C元素的最簡單的氫化物Y的水溶液顯堿性.E是短周期元素中電負性最小的元素。A、B、C、E四種元素都能與D元素形成原子個數(shù)比不相同的常見化合物。試回答下列問題:
(1)寫出A、E兩元素形成的原子個數(shù)比為1:1的化合物的電子式____。
(2)向氯化亞鐵溶液滴加過量的E的最高價氧化物對應水化物的溶液,現(xiàn)象是____。
(3)Y溶液顯堿性的原因是(用一個離子方程式表示)____。
(4)檢驗汽車尾氣中含有的化合物BD的方法是:向酸性PdC12溶液中通A汽車尾氣,若生成黑色沉淀(Pd),證明汽車尾氣中含有BD。寫出反應的離子方程式____。
(5)下列有關物質性質的比較中.不正確的是 。
a.熱穩(wěn)定性:H2S>SiH4 b.離子半徑:Na+>S2-
c.第一電離能N>O d.元素電負性:C>H
(6)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H=+49.0kJ/mol
②CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) △H=-192.9kJ/mol
由上述方程式可知.CH3OH的燃燒熱____(填“大于”、“等于”或小于”)192.9kJ/mol。已知水的氣化熱為44 kJ/mol.則表示氫氣燃燒熱的熱化學方程式為____。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
能源問題日益成為制約國際社會經(jīng)濟發(fā)展的瓶頸,越來越多的國家開始實行“陽光計劃”,開發(fā)太陽能資源,尋求經(jīng)濟發(fā)展的新動力。
(1)太陽能熱水器中常使用一種以鎳或鎳合金空心球為吸收劑的太陽能吸熱涂層,基態(tài)鎳原子M層上的未成對電子數(shù)為 。
(2)大阪大學近日宣布,有機太陽能固體電池效率突破5.3%,而高純度C60是其“秘密武器”。C60的結構如圖1,分子中碳原子軌道的雜化類型為 ;1 mol C60分子中π鍵的數(shù)目為 。
(3)金屬酞菁配合物在硅太陽能電池中有重要作用,一種金屬鎂酞菁配合物的結構如下圖2。該結構中,碳氮之間的共價鍵類型有 (按原子軌道重疊方式填寫共價鍵的類型),請在下圖2中用箭頭表示出配位鍵。

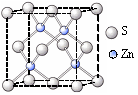
圖1 圖2 圖3
(4)多元化合物薄膜太陽能電池材料為無機鹽,其主要包括砷化鎵、硫化鎘、硫化鋅及銅錮硒薄膜電池等。
①第一電離能:As Se(填“>”、“<”或“=”)。
②硫化鋅的晶胞中(結構如圖所示),硫離子的配位數(shù)是 。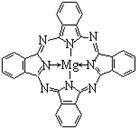
③二氧化硒分子的空間構型為 。
④砷化鎵可由(CH3)3Ga和AsH3在700℃下反應制得,反應的方程式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
已知A、B、C是第二周期的非金屬元素,其原子序數(shù)依次增大,且它們之間可以形成AC和BC以及AC2和BC2分子,D元素是一種短周期元素,它與A、B、C可分別形成電子總數(shù)相等的三種分子。請?zhí)羁眨?br />(1)寫出A、B、C、D對應的元素符號:A________、B________、C________、D________。
(2)寫出工業(yè)生產(chǎn)中BD3與氧氣反應的化學方程式:
________________________________________________________________________。
(3)你認為B、C、D元素形成的化合物之間________(填“能”或“不能”)發(fā)生下面的反應BC+BD3―→DBC2+D2C,得出上面結論的理由是__________________________ _。
(4)Ⅰ.恒溫恒壓下,在一體積可變的密閉容器中發(fā)生下列反應:4AC(g)+2BC2(g)  4AC2(g)+B2(g)在上述條件下,向容器中充入AC和BC2各1 mol達平衡時,生成AC2和B2共a mol,則AC的轉化率是________(用含a的代數(shù)式表示)。
4AC2(g)+B2(g)在上述條件下,向容器中充入AC和BC2各1 mol達平衡時,生成AC2和B2共a mol,則AC的轉化率是________(用含a的代數(shù)式表示)。
Ⅱ. 若維持溫度不變,在一個與Ⅰ反應前的起始體積相同,容積固定的密閉容器中發(fā)生Ⅰ中所述的化學反應,開始時仍向容器中充入AC和BC2各1 mol,達平衡時生成AC2和B2共b mol,將b與Ⅰ中的a進行比較,則a________b(填“>”“<”“=”或“不能確定”)。
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
A、B、C、D、E為原子序數(shù)依次增大的五種短周期元素。A和D最外層電子數(shù)相同;C、E最低負價相同。B、C的最外層電子數(shù)之和等于D的原子核外電子數(shù),A和C可形成兩種常見的化合物甲和乙(相對分子質量甲<乙),D2C中陽離子與陰離子的電子層結構相同。請回答下列問題:
(1)B的氫化物與E的氫化物比較,沸點較高的是 (填化學式)。
(2)已知乙能與由A、C、D組成的化合物的溶液反應,請寫出反應的離子方程式 。
(3)A、B兩種元素可形成一種離子化合物,該離子化合物的電子式為 。
(4)向A、B、C三種元素組成的某鹽溶液中滴加AgNO3溶液生成白色沉淀,該反應的化學方程式為____________。已知該鹽溶液呈酸性,0.1mol·L-1該鹽溶液中離子濃度由大到小的順序是_________________________。
(5)化合物X、Y由A、C、D、E四種元素中的三種組成的強電解質,且兩種物質水溶液的酸堿性相同,組成元素的原子數(shù)目之比均為1∶1∶1,若X能抑制水的電離,Y能促進水的電離,則X與Y反應的離子方程式是 。
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com