
| 過程⑤B溶液中含有的離子 | 過程⑦B溶液中含有的離子 | |
| 甲 | 有Fe3+無Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+無Fe2+ | 有Fe2+ |
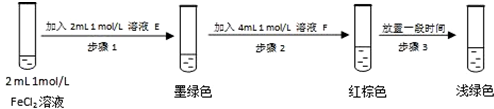
分析 (1)根據大氣壓強原理來檢驗裝置的氣密性:關閉K1、K2,打開分液漏斗的蓋子和活塞,向其中加入水,觀察一段時間后分液漏斗尖嘴處是否滴液;
(2)亞硫酸鈉可以和較濃的硫酸之間反應生成硫酸鈉和水以及二氧化硫;
(3)SO2通入酸性高錳酸鉀溶液,二者之間可以發生氧化還原反應;
(4)裝置A是制備氯氣的,氯氣有毒,要用氫氧化鈉進行吸收,FeCl2溶液容易被O2氧化;
(5)溶液顯酸性,檢驗硫酸根離子應選擇氯化鋇溶液;乙中第一次,說明氯氣不足,氯氣氧化性大于鐵離子,第二次有硫酸根離子,說明發生二氧化硫與鐵離子的反應,則氧化性鐵離子大于二氧化硫丙中第一次有Fe3+,無Fe2+,則氯氣的氧化性大于鐵離子,第二次有亞鐵離子,說明發生二氧化硫與鐵離子的反應,則氧化性鐵離子大于二氧化硫;
(6)①根據已知條件:FeCl3與SO2的反應經歷了中間產物FeSO3,溶液的紅棕色是FeSO3(墨綠色)與FeCl3(黃色)的混合色,所以可以借助氯化鐵和亞硫酸鈉溶液來確定假設是否成立;
②根據化學平衡:Fe2+(aq)+SO32-(aq)?FeSO3(s)(墨綠色),步驟3中,Fe3+消耗SO32-,c(SO32-)減小,平衡逆向移動,溶液顏色由紅棕色變為淺綠色.
解答 解:(1)根據大氣壓強原理來檢驗裝置的氣密性:關閉K1、K2,打開分液漏斗的蓋子和活塞,向其中加入水,一段時間后分液漏斗尖嘴處不再滴液即證明氣密性良好.
故答案為:關閉K1、K2,打開分液漏斗的蓋子和活塞,向其中加入水,一段時間后分液漏斗尖嘴處不再滴液即證明氣密性良好;
(2)亞硫酸鈉可以和較濃的硫酸之間反應生成硫酸鈉和水以及二氧化硫,即Na2SO3+H2SO4=Na2SO4+SO2↑+H2O.
故答案為:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O;
(3)二氧化硫具有還原性,高錳酸鉀具有氧化性,SO2通入酸性高錳酸鉀溶液,二者之間可以發生氧化還原反應:2MnO4-+5SO2+4H2O=2Mn2++5SO42-+4H+,故答案為:2MnO4-+5SO2+4H2O=2Mn2++5SO42-+4H+;
(4)裝置A是制備氯氣的,二氧化錳與濃鹽酸加熱反應生成氯化錳、氯氣和水,氯氣有毒,要用氫氧化鈉進行吸收,由于裝置中含有空氣,而空氣的存在,會對實驗產生干擾,所以通入氮氣的目的是排除裝置中的空氣,防止FeCl2溶液被O2氧化,
故答案為:NaOH溶液;排除裝置中的空氣,防止FeCl2溶液被O2氧化;
(5)溶液顯酸性,檢驗硫酸根離子應選擇氯化鋇溶液;乙中第一次,說明氯氣不足,氯氣氧化性大于鐵離子,第二次有硫酸根離子,說明發生二氧化硫與鐵離子的反應,則氧化性鐵離子大于二氧化硫丙中第一次有Fe3+,無Fe2+,則氯氣的氧化性大于鐵離子,第二次有亞鐵離子,說明發生二氧化硫與鐵離子的反應,則氧化性鐵離子大于二氧化硫;故答案為:乙、丙;
(6)①實驗中溶液顯墨綠色,說明平衡向正反應方向移動,所以加入的應該是Na2SO3(或可溶性亞硫酸鹽);而步驟2中溶液顯紅棕色,說明加入的應該是FeCl3 ,
故答案為:Na2SO3(或可溶性亞硫酸鹽);FeCl3;
②由于Fe3+消耗 SO32-,c(SO32-)減小,使平衡Fe2+(aq)+SO32-(aq)?FeSO3(s)逆向移動,溶液顏色由紅棕色變為淺綠色,
故答案為:Fe3+消耗 SO32-,c(SO32-)減小,使平衡Fe2+(aq)+SO32-(aq)?FeSO3(s)逆向移動,溶液顏色由紅棕色變為淺綠色.
點評 本題考查性質實驗方案的設計,涉及了氧化還原反應的判斷、化學實驗基本操作方法、氯氣的制備、氯氣、氯化鐵和SO2性質的探究以及外界條件對平衡狀態的影響等知識,題目難度中等,明確裝置的作用及發生的反應是解答的關鍵,注意氧化性的比較是解答的難點.


科目:高中化學 來源: 題型:選擇題
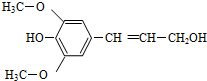 膳食纖維具有的突出保健功能,近年來受到人們的普遍關注,被世界衛生組織稱為人體的“第七營養素”.木質素是一種非糖類膳食纖維,其單體之一是芥子醇,結構如圖所示.下列有關芥子醇的說法正確的是( )
膳食纖維具有的突出保健功能,近年來受到人們的普遍關注,被世界衛生組織稱為人體的“第七營養素”.木質素是一種非糖類膳食纖維,其單體之一是芥子醇,結構如圖所示.下列有關芥子醇的說法正確的是( )| A. | 芥子醇的分子式是C11H12O4 | |
| B. | 芥子醇分子中所有碳原子可能在同一平面 | |
| C. | 1mol芥子醇能與足量溴水反應消耗3molBr2 | |
| D. | 1mol芥子醇與足量的氫氣反應消耗氫氣4mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 工業制硫酸時用到的主要設備有沸騰爐、接觸室、吸收塔 | |
| B. | 可用KSCN溶液檢驗某溶液中是否存在Fe3+ | |
| C. | 相同條件下同體積同濃度的鹽酸分別與等質量的碳酸鈉、碳酸氫鈉固體反應,后者速率快 | |
| D. | 鋁粉可與氧化鎂在高溫下發生鋁熱反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 增大反應物濃度可以增大活化分子百分數,從而使反應速率增大 | |
| B. | 汽車尾氣的催化轉化裝置可將尾氣中的NO和CO等有害氣體快速地轉化為N2和CO2,其原因是催化劑可增大NO和CO反應的活化能 | |
| C. | 在“反應熱的測量實驗”中測定反應后溫度的操作方法:將量筒中的NaOH溶液經玻璃棒引流緩緩倒入盛有鹽酸的簡易量熱計中,立即蓋上蓋板,并用環形玻璃攪拌棒不斷攪拌,準確讀出并記錄反應體系的最高溫度 | |
| D. | 研制性能優良的催化劑既可以提高化學反應速率,又能起到很好的節能效果 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
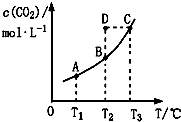
| A. | 該反應的△H<0 | |
| B. | 在T2時,D點的反應速率:ν(正)<(逆) | |
| C. | A、C兩點相比,混合氣體的平均相對分子質量:M(A)<M(C) | |
| D. | 若T1、T2時的平衡常數分別為K1、K2,則K1>K2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | K+、Ca2+、HCO3-、Br- | B. | SO32-、Al(OH)4-、K+、Al3+ | ||
| C. | Fe3+、Na+、NO3-、CO32- | D. | NH4+、Na+、SiO32-、I- | ||
| E. | Ca2+、Na+、NO3-、PO43- |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com