

 (不考慮空間構型,如有配位鍵,請標出)
(不考慮空間構型,如有配位鍵,請標出)分析 Q、R、X、Y、Z五種元素的原子序數依次遞增,Z的原子序數為29,則Z為Cu元素,其余的均為短周期主族元素;
Q、X原子p軌道的電子數分別為2和4,Q原子的核外電子排布為1s22s22p2,故Q為C元素,X原子的核外電子排布為1s22s22p4,則X為O元素;
Y原子價電子(外圍電子)排布msnmpn,n=2,故為第ⅣA族元素,其原子序數大于O元素,小于Cu元素,故Y為Si元素;
R原子核外L層電子數為奇數,R原子有2個電子層,原子序數介于C元素與O元素之間,故R為N元素,
再結合題目分析解答.
解答 解:Q、R、X、Y、Z五種元素的原子序數依次遞增,Z的原子序數為29,則Z為Cu元素,其余的均為短周期主族元素;
Q、X原子p軌道的電子數分別為2和4,Q原子的核外電子排布為1s22s22p2,故Q為C元素,X原子的核外電子排布為1s22s22p4,則X為O元素;
Y原子價電子(外圍電子)排布msnmpn,n=2,故為第ⅣA族元素,其原子序數大于O元素,小于Cu元素,故Y為Si元素;
R原子核外L層電子數為奇數,R原子有2個電子層,原子序數介于C元素與O元素之間,故R為N元素,
(1)C、N、O、Si、Cu元素基態時未成對電子數分別是2、3、2、2、1,所以五種元素原子中基態時未成對電子數最多的是N元素,故答案為:N;
(2)Y是Si元素,其1s、2s、2p、3s、3p能級分別有2、2、6、2、2個電子,基態原子Si的軌道表示式是: ,
,
故答案為: ;
;
(3)Z是Cu元素,其原子核外有29個電子,根據構造原理知,基態原子Cu的電子排布式是1s22s22p63s23p63d104s1,向Z的硫酸鹽溶液中加入過量氨水時生成銅銨絡離子,反應的離子方程式是Cu 2++4NH3.H2O=Cu(NH3)42++4H2O,配合物離子[Cu(NH3)4]2+中的配位鍵為 ;
;
故答案為:1s22s22p63s23p63d104s1;Cu 2++4NH3.H2O=Cu(NH3)42++4H2O; ;
;
(4)Q、R、X分別是C、N、O元素,同一周期元素,其電負性隨著原子序數增大而增大,所以Q、R、X的電負性由小到大的順序是C、N、O,故答案為:C、N、O;
(5)Q、X和Y分半是C、O、Si元素,元素的非金屬性越強,其氫化物的穩定性越強,非金屬性O>C>Si,所以Q、X、Y的氫化物穩定性由小到大的順序為SiH4<CH4<H2O,故答案為:SiH4<CH4<H2O;
(6)在一定條件下,原子從能量高的能級躍遷到能量低的能級時放出能量,所以原子的核外電子從激發態躍遷到基態產生的光譜屬于發射光譜(填“吸收”或“發射”),該光譜可用于鑒定元素,
故答案為:發射;鑒定.
點評 本題考查物質結構和性質相互關系及應用,為高頻考點,涉及元素周期律、配合物結構、原子核外電子排布等知識點,綜合性較強,側重考查學生知識綜合運用能力,注意配位鍵的表示方法,題目難度不大.


 黃岡天天練口算題卡系列答案
黃岡天天練口算題卡系列答案科目:高中化學 來源: 題型:選擇題
| A. | 加入AgNO3溶液,生成白色沉淀,加稀鹽酸沉淀不消失,可確定有Cl-存在 | |
| B. | 加入鹽酸,生成的氣體能使澄清石灰水變渾濁,可確定有CO32-存在 | |
| C. | 加入Ba(NO3)2,生成白色沉淀,加稀鹽酸沉淀不消失,可確定有SO42-存在 | |
| D. | 用潔凈的鉑絲蘸取溶液放在火焰上灼燒,觀察到火焰呈黃色,可確定有Na+存在 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | a=b+c | B. | a=b-c | C. | a=c-b | D. | c=a+b |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Ca2+[:$\underset{\stackrel{••}{Cl}}{••}$:]2- | B. | Na+[$\stackrel{•}{X}$$\underset{\stackrel{••}{S}}{••}$$\stackrel{•}{X}$]-2Na+ | ||
| C. | [Mg2+][$\underset{X}{•}$$\underset{\stackrel{••}{O}}{••}$$\underset{X}{•}$]2- | D. | K+[$\stackrel{•}{X}$$\underset{\stackrel{••}{F}}{••}$:]- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
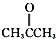 ③CH3CH2Br ④
③CH3CH2Br ④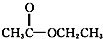 ⑤
⑤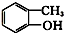
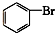 ⑦
⑦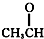 ⑧
⑧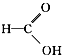 ⑨
⑨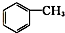 ⑩
⑩
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
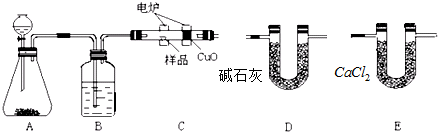
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | -(a-b)kJ•mol-1 | B. | -(a+b)kJ•mol-1 | ||
| C. | -(5a-0.5b)kJ•mol-1 | D. | -(0.5a-5b)kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
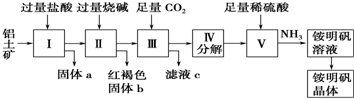
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
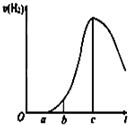 某化學小組進行了關于“活潑金屬與酸反應”的實驗,得出了一些有趣的想法,請你幫助他們,完成一些判斷.將5.4g鋁片投入500mL 0.5mol•L-1的硫酸溶液中,下圖為反應產氫速率與反應時間的關系圖.
某化學小組進行了關于“活潑金屬與酸反應”的實驗,得出了一些有趣的想法,請你幫助他們,完成一些判斷.將5.4g鋁片投入500mL 0.5mol•L-1的硫酸溶液中,下圖為反應產氫速率與反應時間的關系圖.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com