
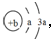 ,Y、Z為同周期金屬元素,其中Y為短周期元素中原子半徑最大的元素,Z為地殼中含量最高的金屬元素,W的最高價氧化物對應水化物可以與其氣態氫化物反應生成鹽G,鹽G溶液呈酸性,回答下列問題:
,Y、Z為同周期金屬元素,其中Y為短周期元素中原子半徑最大的元素,Z為地殼中含量最高的金屬元素,W的最高價氧化物對應水化物可以與其氣態氫化物反應生成鹽G,鹽G溶液呈酸性,回答下列問題: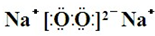 ,所含有的化學鍵類型為離子鍵和共價鍵.
,所含有的化學鍵類型為離子鍵和共價鍵.分析 X的原子結構示意圖為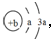 ,可知a=2,b=8,則X為O元素,Y、Z為同周期金屬元素,其中Y為短周期元素中原子半徑最大的元素,應為Na,Z為地殼中含量最高的金屬元素,應為Al,W的最高價氧化物對應水化物可以與其氣態氫化物反應生成鹽G,鹽G溶液呈酸性,則W為N元素,G為NH4NO3,結合對應單質、化合物的性質以及元素周期率知識解答該題.
,可知a=2,b=8,則X為O元素,Y、Z為同周期金屬元素,其中Y為短周期元素中原子半徑最大的元素,應為Na,Z為地殼中含量最高的金屬元素,應為Al,W的最高價氧化物對應水化物可以與其氣態氫化物反應生成鹽G,鹽G溶液呈酸性,則W為N元素,G為NH4NO3,結合對應單質、化合物的性質以及元素周期率知識解答該題.
解答 解:(1)由以上分析可知X為O元素,W為N元素,位于周期表第二周期ⅤA族,同周期元素從左到右原子半徑逐漸減小,且核外電子層數越多,原子半徑越大,四種元素的原子半徑從大到小的順序是Na>Al>N>O,
故答案為:O;第二周期ⅤA族;Na>Al>N>O;
(2)Y2X2為淺黃色固體物質,應為過氧化鈉,電子式為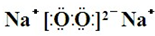 ,含有離子鍵和共價鍵,
,含有離子鍵和共價鍵,
故答案為: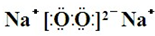 ;離子鍵和共價鍵;
;離子鍵和共價鍵;
(3)Y的最高價氧化物對應水化物為氫氧化鈉,與鋁的單質反應的離子方程式為2Al+2H2O+2OH-=2AlO2-+3H2↑,
故答案為:2Al+2H2O+2OH-=2AlO2-+3H2↑.
點評 本題考查結構性質位置關系應用,為高頻考點和常見題型,側重考查學生的分析能力,推斷元素是解題關鍵,注意對元素周期律與元素化合物性質掌握.


 同步練習強化拓展系列答案
同步練習強化拓展系列答案科目:高中化學 來源: 題型:選擇題
| A. | 同溫度、同濃度的NaCl溶液和氨水的導電能力 | |
| B. | 25℃時.pH均為2的鹽酸和CH3COOH溶液中溶質的物質的量濃度 | |
| C. | 25℃時,pH均為2的H2SO4溶液和鹽酸中氫離子的物質的量濃度 | |
| D. | 25℃時.pH均為3的鹽酸和FeCI3溶液中水的電離程度 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 若二氧化碳氣體中混有少量的一氧化碳氣體,可用點燃的方法除去 | |
| B. | 將銅粉中混有的少量鐵粉除去,加入過量的CuSO4溶液充分反應后,過濾、洗滌干燥 | |
| C. | 將KNO3固體中混有的少量NaCl固體除去,可以用冷卻KNO3的熱飽和溶液、過濾即可 | |
| D. | 若氧氣中混有少量的二氧化碳氣體,可將混合氣體通過足量的NaOH溶液后干燥 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Fe═Fe2++2e- | B. | Cu2++2e-═Cu | C. | Fe═Fe3++3e- | D. | Zn═Zn2++2e- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
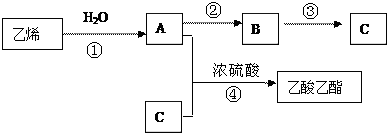
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
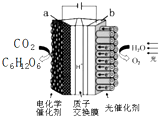 中關村“創客19”實驗室模擬光合作用的電化學實驗裝置如右圖所示,該裝置能將H2O和CO2轉化為O2和葡萄糖(C6H12O6).下列說法正確的是( )
中關村“創客19”實驗室模擬光合作用的電化學實驗裝置如右圖所示,該裝置能將H2O和CO2轉化為O2和葡萄糖(C6H12O6).下列說法正確的是( )| A. | 該裝置是新型化學電源裝置 | |
| B. | 該裝置工作時,H+從a極區向b極區遷移 | |
| C. | 每生成1 mol O2,有44 g CO2被還原 | |
| D. | a 電極的反應為:6CO2+24H+-24e-=C6H12O6+6 H2 O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 苯、乙醇、四氯化碳都是重要有機溶劑,都可用于提取碘水中的碘單質 | |
| B. | 在強堿性溶液中,[Al(OH)4]-、HCO3-、Na+、Ca2+可能同時大量共存 | |
| C. | 鐵船底鑲嵌鋅塊,構成原電池,鋅作負極,以防船體被腐蝕 | |
| D. | 用量筒量取10.mL 1.0mol/L的鹽酸于100mL溶液瓶中,加水稀釋至刻度,可制得0.1mol/L的鹽酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下pH=13的溶液中:NH4+、Na+、Cl-、CO32- | |
| B. | 能與金屬鋁反應放出氫氣的溶液中:K+、NO3-、Cl-、NH4+ | |
| C. | 能夠與金屬Cu常溫下反應放出氣體的溶液:Na+、Al3+、SO42-、K+ | |
| D. | 漂白粉的水溶液中:Fe2+、Cl-、Ca2+、Na+ |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
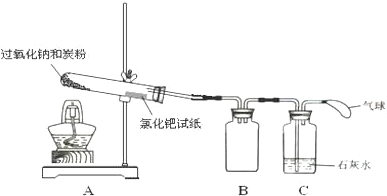
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com