
 某Na2CO3、NaAlO2的混合溶液中逐滴加入1mol•L-1的鹽酸,測得溶液中的CO32-、HCO3-、AlO2-、Al3+的物質的量與加入鹽酸溶液的體積變化關系如圖所示.則下列說法不正確的是( )
某Na2CO3、NaAlO2的混合溶液中逐滴加入1mol•L-1的鹽酸,測得溶液中的CO32-、HCO3-、AlO2-、Al3+的物質的量與加入鹽酸溶液的體積變化關系如圖所示.則下列說法不正確的是( )| A. | M點時生成的CO2為0mol | |
| B. | 原混合溶液中的CO32-與AlO2-的物質的量之比為1:1 | |
| C. | V1:V2=1:3 | |
| D. | a曲線表示的離子方程式為:AlO2-+H++H2O=Al(OH)3↓ |
分析 Na2CO3、NaAlO2的混合溶液中逐滴加入1mol•L-1的鹽酸后,首先發生反應:AlO2-+H++H2O═Al(OH)3↓,a曲線表示AlO2-,由圖可知AlO2-反應完畢,加入鹽酸50mL,根據方程式可知:n(AlO2-)=n(H+)=0.05mol×1mol/L=0.05mol;
AlO2-反應完畢,發生反應:CO32-+H+═HCO3-,b曲線表示CO32-,c曲線表示HCO3-,由圖可知CO32-反應完畢,該階段加入鹽酸100mL-50mL=50mL,根據方程式可知:n(CO32-)=n(H+)=0.05mol×1mol/L=0.05mol;
CO32-反應完畢,發生反應HCO3-+H+═CO2↑+H2O,d曲線表示HCO3-,由圖可知HCO3-反應完畢,該階段加入鹽酸150mL-100mL=50mL,根據方程式可知n(HCO3-)=n(H+);
發生反應Al(OH)3+3H+═Al3++3H2O,e曲線表示Al3+,由圖可知Al(OH)3反應完畢,根據方程式可知n(H+)=3n[Al(OH)3]=3×0.05mol=0.15mol,進而求出消耗鹽酸的體積.
解答 解:Na2CO3、NaAlO2的混合溶液中逐滴加入1mol•L-1的鹽酸,先發生的反應為:AlO2-+H++H2O═Al(OH)3↓,則a曲線表示AlO2-,由圖可知AlO2-反應完畢,加入鹽酸50mL,根據方程式可知:n(AlO2-)=n(H+)=0.05mol×1mol/L=0.05mol;
AlO2-反應完畢后發生反應:CO32-+H+═HCO3-,b曲線表示CO32-,c曲線表示HCO3-,由圖可知CO32-反應完畢,該階段加入鹽酸體積為:100mL-50mL=50mL,根據方程式可知:n(CO32-)=n(H+)=0.05mol×1mol/L=0.05mol;
CO32-反應完后又發生反應:HCO3-+H+═CO2↑+H2O,d曲線表示HCO3-,由圖可知HCO3-反應完畢,該階段加入鹽酸體積為:150mL-100mL=50mL,根據方程式可知:n(HCO3-)=n(H+)=0.05mol;
最后發生反應為:Al(OH)3+3H+═Al3++3H2O,e曲線表示Al3+,由圖可知Al(OH)3反應完畢,根據方程式可知:n(H+)=3n[Al(OH)3]=3×0.05mol=0.15mol,該階段加入鹽酸體積為:$\frac{0.15mol}{1mol/L}$=0.15L=150mL;
A.根據述分析可知,M點時溶液中CO32-完全轉化為HCO3-,沒有CO2生成,故A正確;
B.由上述分析可知,原混合溶液中的CO32-與AlO-2的物質的量之比為:0.05mol:0.05mol=1:1,故B正確;
C.原溶液中n(CO32-)=0.05mol,V1時溶液中碳酸氫根離子等于碳酸根離子為0.025ml,由反應CO32-+H+═HCO3-可知,需要鹽酸為0.025mol,鹽酸的體積為25mL,故V1=50mL+25mL=75mL,由上述分析可知,V2=150mL+150mL=300mL,故V1:V2=75mL:300mL=l:4,故C錯誤;
D.由上述分析可知,a曲線表示的離子方程式為:AlO-2+H++H2O=Al(OH)3↓,故D正確;
故選C.
點評 本題結合圖象曲線考查了有關混合物反應的計算,題目難度較大,明確離子性質及反應的先后順序為解答關鍵,試題側重考查對圖象曲線的分析、理解能力及化學計算能力.


 學而優銜接教材南京大學出版社系列答案
學而優銜接教材南京大學出版社系列答案 小學課堂作業系列答案
小學課堂作業系列答案 金博士一點全通系列答案
金博士一點全通系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | BaCl2 Na2CO3 AgNO3 鹽酸 | B. | BaCl2 Na2CO3 鹽酸 AgNO3 | ||
| C. | Na2CO3 鹽酸 AgNO3 BaCl2 | D. | AgNO3 鹽酸 BaCl2 Na2CO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該反應達到平衡時,放出的熱量等于92.4kJ | |
| B. | 達到平衡后向容器中通入1mol氦氣,平衡向左移動 | |
| C. | 降低溫度和縮小容器體積均可使該反應的平衡常數增大 | |
| D. | 若達到平衡時N2的轉化率為20%,則平衡時容器內的壓強是起始時的90% |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | n(Cl2):n(Fe)=5:4 5Cl2+4Fe$\frac{\underline{\;點燃\;}}{\;}$2FeCl2+2FeCl3 | |
| B. | n(Cl2):n(FeBr2)=1:1 Fe2++2Br-+Cl2═Fe3++Br2+2Cl- | |
| C. | n(MnO4-):n(H2O2)=2:3 2MnO4-+3H2O2+6H+═2Mn2++4O2↑+6H2O | |
| D. | n(Fe):n(HNO3(稀))═1:3 4Fe+12H++3NO3-=3Fe2++Fe3++3NO↑+6H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ⑩ | ① | ② | ③ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
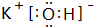 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com