
【題目】工業純堿中常常含有NaCl、![]() 等雜質。為測定某工業純堿的純度。設計了如圖實驗裝置。依據實驗設計,請回答:
等雜質。為測定某工業純堿的純度。設計了如圖實驗裝置。依據實驗設計,請回答:

(1)儀器D的名稱是______________;裝置D的作用是______________________。
(2)若不考慮操作、藥品及其用量等方面的影響,該實驗測得結果會___________(填“偏高”、“偏低”,“無影響”)。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
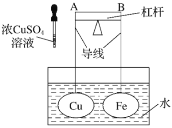
【題目】如圖所示,杠桿AB兩端分別掛有體積相同、質量相等的空心銅球和空心鐵球,調節杠桿并使其在水中保持平衡,然后小心地向水槽中滴入濃![]() 溶液,一段時間后,下列有關杠桿的偏向判斷正確的是(實驗中,不考慮兩球的浮力變化)( )
溶液,一段時間后,下列有關杠桿的偏向判斷正確的是(實驗中,不考慮兩球的浮力變化)( )
A.杠桿為導體或絕緣體時,均為A端高B端低
B.杠桿為導體或絕緣體時,均為A端低B端高
C.當杠桿為導體時,A端高B端低;杠桿為絕緣體時,A端低B端高
D.當杠桿為導體時,A端低B端高;杠桿為絕緣體時,A端高B端低
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用表示阿伏加德羅常數的值,下列敘述不正確的是
A.4.6gNa與含0.1molHCl的稀鹽酸充分反應,轉移電子數目為0.2![]()
B.25℃時,1L![]() 的
的![]() 溶液中由水電離的的數目為
溶液中由水電離的的數目為![]()
C.常溫常壓下,![]() 和
和![]() 混合氣體所含的原子數為
混合氣體所含的原子數為![]()
D.500℃時,![]() 和
和![]() 在密閉容器中充分反應后生成
在密閉容器中充分反應后生成![]() 的分子數為
的分子數為![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】120℃時,1molCO2和3molH2通入1L的密閉容器中反應生成CH3OH和水。測得CO2和CH3OH的濃度隨時間的變化如圖所示。下列有關說法中不正確的是

A.0~3min內,H2的平均反應速率為0.5mol·L-1·min-1
B.該反應的化學方程式:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)
C.容器內氣體的壓強不再變化時,反應到達平衡
D.10min后,反應體系達到平衡
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】烴是只含碳氫元素的一類有機物,關于下列烴的說法正確的是()
|
| CH3CH2CH2CH2CH2CH3 |
|
A.名稱 1,3,4–三甲苯 | B.名稱 2,2–二乙基丁烷 | C.所有碳原子可能處于同一平面 | D.所有碳原子一定處于同一平面 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物X是一種烷烴,是液化石油氣的主要成分,可通過工藝Ⅰ的兩種途徑轉化為A和B、C和D。B是一種重要的有機化工原料,E分子中含環狀結構,F中含有兩個相同的官能團,D是常見有機物中含氫量最高的,H能使![]() 溶液產生氣泡,Ⅰ是一種有濃郁香味的油狀液體。
溶液產生氣泡,Ⅰ是一種有濃郁香味的油狀液體。
請回答:
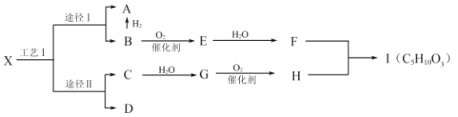
(1)G的結構簡式為_________________________。
(2)G→H的反應類型是_________________________。
(3)寫出F+H→1的化學方程式_________________________。
(4)下列說法正確的是_______。
A.工藝Ⅰ是石油的裂化
B.除去A中的少量B雜質,可在一定條件下往混合物中通入適量的氫氣
C.X、A、D互為同系物,F和甘油也互為同系物
D.H與![]() 互為同分異構體
互為同分異構體
E.等物質的量的Ⅰ和B完全燃燒,消耗氧氣的質量比為2:1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國科研人員以Zn和尖晶石型錳酸鋅(ZnMn2O4)為電極材料,研制出一種水系鋅離子電池。該電池的總反應方程式:xZn + Zn1xMn2O4![]() ZnMn2O4(0 < x < 1)。下列說法正確的是
ZnMn2O4(0 < x < 1)。下列說法正確的是
A. 充電時,Zn2+向ZnMn2O4電極遷移
B. 充電時,陽極反應:ZnMn2O4 2xe—=Zn1-xMn2O4+xZn2+
C. 放電時,每轉移1mol e-,ZnMn2O4電極質量增加65g
D. 充放電過程中,只有Zn元素的化合價發生變化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】三氯胺(![]() )是一種飲用水二級消毒劑,可由以下反應制備:Ⅰ.
)是一種飲用水二級消毒劑,可由以下反應制備:Ⅰ.![]()
![]() 。回答下列問題:
。回答下列問題:
(1)已知:Ⅱ.![]()
![]() Ⅲ.
Ⅲ.![]()
![]() ,則
,則![]() ________(用含
________(用含![]() 和
和![]() 的代數式表示)。
的代數式表示)。
(2)向容積均為2 L的甲、乙兩個恒溫密閉容器中分別加入![]() 和
和![]() ,發生反應Ⅰ,測得兩容器中
,發生反應Ⅰ,測得兩容器中![]() 隨反應時間的變化情況如下表所示:
隨反應時間的變化情況如下表所示:
時間/min | 0 | 40 | 80 | 120 | 160 |
容器甲( | 4.0 | 3.0 | 2.2 | 1.6 | 1.6 |
容器乙( | 4.0 | 2.9 | 2.0 | 2.0 | 2.0 |
①0~80 min內,容器甲中![]() ________。
________。
②反應Ⅰ的![]() ________0(填“>”或“<”),其原因為________________________。
________0(填“>”或“<”),其原因為________________________。
③關于反應Ⅰ,下列說法正確的是________(填選項字母)。
a.容器內![]() ,說明反應達到平衡狀態
,說明反應達到平衡狀態
b.容器內氣體密度不變,說明反應達到平衡狀態
c.達平衡后,加人一定量![]() ,平衡逆向移動
,平衡逆向移動
d.達平衡后,按原投料比再充入一定量反應物,平衡后![]() 的轉化率增大
的轉化率增大
④溫度為![]() 時HCl(g)的平衡體積分數=________,該溫度下,若改為初始體積為2 L的可變容器,平衡時容器中
時HCl(g)的平衡體積分數=________,該溫度下,若改為初始體積為2 L的可變容器,平衡時容器中![]() ________(填“>”“=”或“<”)1.6 mol。
________(填“>”“=”或“<”)1.6 mol。
⑤溫度為![]() 時,該反應的平衡常數
時,該反應的平衡常數![]() ________。
________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有8種物質:①甲烷 ②苯 ③聚乙烯 ④聚異戊二烯(![]() ) ⑤2-丁炔 ⑥環乙烷 ⑦鄰二甲苯 ⑧2-甲基-1,3-丁二烯,既能使酸性高錳酸鉀溶液褪色,又能與溴水反應使之褪色的是
) ⑤2-丁炔 ⑥環乙烷 ⑦鄰二甲苯 ⑧2-甲基-1,3-丁二烯,既能使酸性高錳酸鉀溶液褪色,又能與溴水反應使之褪色的是
A. ③④⑤⑧ B. ④⑤⑦⑧ C. ④⑤⑧ D. ③④⑤⑦⑧
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com