
| A. | 配制鹽酸用量筒量取鹽酸時俯視刻度線 | |
| B. | 配制鹽酸定容時,仰視容量瓶刻度線 | |
| C. | 稱量20gNaOH來配制0.5 mol•L-1 NaOH溶液1000 mL 時,砝碼錯放在左盤 | |
| D. | NaOH溶解后未經冷卻即注入容量瓶至刻度線 |
分析 A.俯視量筒刻度線導致量取鹽酸的體積偏小,所配溶液濃度偏低;
B.定容時仰視容量瓶刻度線,導致液體體積偏大,所配溶液濃度偏低;
C.砝碼錯放在左盤,稱量的氫氧化鈉質量偏低,配制的溶液濃度偏低;
D.NaOH溶解后未經冷卻即注入容量瓶至刻度線,導致溶液體積偏小,所配溶液濃度偏高.
解答 解:A.用量筒量取鹽鹽酸時,俯視刻度線導致量取鹽酸的體積偏小,所配溶液中溶質的物質的量偏小,溶液濃度偏低,故A錯誤;
B.定容時仰視容量瓶刻度線,導致配制的鹽酸體積偏大,所得溶液的濃度會偏低,故B錯誤;
C.稱量氫氧化鈉時砝碼錯放在左盤,導致稱取的NaOH固體的質量偏小,配制的溶液濃度偏小,故C錯誤;
D.NaOH溶解后未經冷卻即注入容量瓶至刻度線,導致所得溶液的體積偏小,所配溶液濃度偏高,故D正確;
故選D.
點評 本題考查了配制一定物質的量濃度的溶液方法及誤差分析,題目難度不大,明確配制步驟為解答關鍵,注意掌握誤差分析的方法與技巧,試題培養了學生的 化學實驗能力.


 科學實驗活動冊系列答案
科學實驗活動冊系列答案科目:高中化學 來源: 題型:選擇題
| A. | 將SO2氣體通入足量澄清石灰水 | |
| B. | 在Na2S溶液中通入SO2氣體直至過過量 | |
| C. | 在Na2SO3溶液中通入H2S氣體直至過量 | |
| D. | 將8.7克MnO2固體與含0.4mol溶質的濃鹽酸加熱并充分反應后 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鐵在氯氣中燃燒,生成棕紅色的煙 | |
| B. | 紅熱的銅絲在氯氣里劇烈燃燒,生成棕黃色的煙 | |
| C. | 純凈的H2在Cl2中安靜地燃燒,發出蒼白色火焰,集氣瓶口呈現白色煙霧 | |
| D. | 氯氣能與水反應生成次氯酸和鹽酸,久置氯水最終變為稀鹽酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
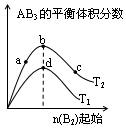 某化學小組研究在其他條件不變時,改變密閉容器中某一條件對A2(g)+3B2(g)?2AB3(g)化學平衡狀態的影響,得到如圖所示的曲線(圖中T表示溫度,n表示物質的量)下列判斷正確的是( )
某化學小組研究在其他條件不變時,改變密閉容器中某一條件對A2(g)+3B2(g)?2AB3(g)化學平衡狀態的影響,得到如圖所示的曲線(圖中T表示溫度,n表示物質的量)下列判斷正確的是( )| A. | 圖中T2一定大于T1 | |
| B. | 圖中b點速率一定大于d點速率 | |
| C. | 達到平衡時,A2的轉化率大小為:c>b>a | |
| D. | 加入催化劑可以使狀態d變為狀態b |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com