
分析 (1)①實驗室利用氯化銨與氫氧化鈣再加熱條件下制備氨氣,反應生成氯化鈣、氨氣與水;
②濃硝酸見光分解生成二氧化氮與氧氣、水;
③二氧化氮和水反應是硝酸與NO;
(2)①若A、B、C、D均為化合物,而且它們的水溶液均能使濕潤的藍色石蕊試紙變紅,它們的水溶液均呈酸性,則A為H2S,B為SO2,C為SO3,D為H2SO4;
②若A的水溶液能使濕潤的紅色石蕊試紙變藍,則A為NH3,D的稀溶液能使濕潤的藍色石蕊試紙變紅,D呈酸性,則B為NO,C為NO2,D為HNO3;
③若A為單質,組成元素的原子所含質子的數目小于18,D為強堿,則A為Na,B為Na2O,C為Na2O2,D為NaOH.
解答 解:(1)①實驗室利用氯化銨與氫氧化鈣再加熱條件下制備氨氣,反應生成氯化鈣、氨氣與水,反應方程式為:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,
故答案為:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
②濃硝酸見光分解生成二氧化氮與氧氣、水,反應方程式為:4HNO3 $\frac{\underline{\;\;△\;\;}}{\;}$O2+4NO2↑+2H2O,
故答案為:4HNO3 $\frac{\underline{\;\;△\;\;}}{\;}$O2+4NO2↑+2H2O;
③二氧化氮和水反應是硝酸與NO,反應方程式為:3NO2+H2O═NO+2HNO3,
故答案為:3NO2+H2O═NO+2HNO3;
(2)①若A、B、C、D均為化合物,而且它們的水溶液均能使濕潤的藍色石蕊試紙變紅,它們的水溶液均呈酸性,則A為H2S,B為SO2,C為SO3,D為H2SO4,B→C的化學方程式:2SO2+O2$\frac{\underline{\;催化劑\;}}{△}$2SO3,
故答案為:H2SO4;2SO2+O2$\frac{\underline{\;催化劑\;}}{△}$2SO3;
②若A的水溶液能使濕潤的紅色石蕊試紙變藍,則A為NH3,D的稀溶液能使濕潤的藍色石蕊試紙變紅,D呈酸性,則B為NO,C為NO2,D為HNO3,A→B的化學方程式:4NH3+5O2$\frac{\underline{\;催化劑\;}}{△}$4NO+6H2O,
故答案為:HNO3;4NH3+5O2$\frac{\underline{\;催化劑\;}}{△}$4NO+6H2O;
③若A為單質,組成元素的原子所含質子的數目小于18,D為強堿,則A為Na,B為Na2O,C為Na2O2,D為NaOH,C→D的化學方程式:2Na2O2+2H2O═4NaOH+O2↑,
故答案為:2Na2O2+2H2O═4NaOH+O2↑.
點評 本題考查無機物推斷,涉及S、N、Na元素及其化合物的性質與轉化,需要學生熟練掌握元素化合物性質,難度不大.


科目:高中化學 來源: 題型:解答題
 有一透明溶液,已知其中可能含有Fe3+、Mg2+、Cu2+、Al3+、NH4+,加入一種淡黃色粉末固體時,加熱有刺激性氣味的混合氣體放出,同時生成白色沉淀.當加入0.4mol淡黃色粉末時,產生氣體0.3mol,繼續加入淡黃色粉末時,產生無刺激性氣味的氣體,且加入淡黃色粉末時產生白色沉淀的量如圖所示.
有一透明溶液,已知其中可能含有Fe3+、Mg2+、Cu2+、Al3+、NH4+,加入一種淡黃色粉末固體時,加熱有刺激性氣味的混合氣體放出,同時生成白色沉淀.當加入0.4mol淡黃色粉末時,產生氣體0.3mol,繼續加入淡黃色粉末時,產生無刺激性氣味的氣體,且加入淡黃色粉末時產生白色沉淀的量如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
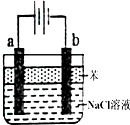 (1)用惰性電極電解飽和食鹽水的反應方程式為:2NaCl+2H2O$\frac{\underline{\;電解\;}}{\;}$2NaOH+H2↑+Cl2↑.
(1)用惰性電極電解飽和食鹽水的反應方程式為:2NaCl+2H2O$\frac{\underline{\;電解\;}}{\;}$2NaOH+H2↑+Cl2↑.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | SO2、H2S、O2 | B. | CO、H2、Cl2 | C. | NO、H2、O2 | D. | HCl、CO、NH3 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

 (或寫成
(或寫成 R代表取代基或氫)
R代表取代基或氫) .
. .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com