
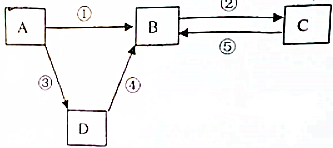
分析 根據題中各物質轉化關系,
(1)若A是太陽能電池用的光伏材料,判斷A為Si.B、C為鈉鹽,C廣泛用于玻璃、造紙等工業,則C為Na2CO3,B為Na2SiO3,則D為SiO2;
(2)若A是淡黃色固體,B是造成酸雨的主要物質之一,則A為S,B為SO2,D是氫化物,則D為H2S,②反應是SO2的水溶液中通入一種黃綠色氣體為氯氣,生成硫酸和鹽酸,符合題中各物質轉化關系;
(3)若B是氣態氫化物.B、C是氧化物且會造成光化學煙霧污染,判斷為NO、NO2,氮氣與氧氣反應生成一氧化氮,所以B為NO,C為NO2,B與C在一定條件下反應生成的A是大氣主要成分,推斷A為N2,D為NH3,依據推斷出的物質書寫化學方程式.
解答 解:(1)若A是太陽能電池用的光伏材料,判斷A為Si.B、C為鈉鹽,C廣泛用于玻璃、造紙等工業,則C為Na2CO3,B為Na2SiO3,則D為SiO2,反應①的離子方程式為Si+2OH-+H2O=SiO32-+2H2↑,反應⑤的化學方程式為Na2CO3+SiO2$\frac{\underline{\;高溫\;}}{\;}$Na2SiO3+CO2 ↑,
故答案為:Na2CO3;Si+2OH-+H2O=SiO32-+2H2↑;Na2CO3+SiO2$\frac{\underline{\;高溫\;}}{\;}$Na2SiO3+CO2 ↑;
(2)若A是淡黃色固體,B是造成酸雨的主要物質之一,則A為S,B為SO2,D是氫化物,則D為H2S,②反應是SO2的水溶液中通入一種黃綠色氣體為氯氣,生成硫酸和鹽酸,反應④的化學方程式為2H2S+3O2$\frac{\underline{\;點燃\;}}{\;}$2SO2+2H2O,
故答案為:2H2S+3O2$\frac{\underline{\;點燃\;}}{\;}$2SO2+2H2O;
(3)若B是氣態氫化物.B、C是氧化物且會造成光化學煙霧污染,判斷為NO、NO2,氮氣與氧氣反應生成一氧化氮,所以B為NO,C為NO2,B與C在一定條件下反應生成的A是大氣主要成分,推斷A為N2,D為NH3,③反應的化學方程式為為N2+3H2$?_{催化劑}^{高溫高壓}$2NH3,NH3與NO在催化劑加熱條件下反應生成氮氣的化學方程式為4NH3+6NO$\frac{\underline{催化劑}}{△}$5N2+6H2O,
故答案為:4NH3+5O2$\frac{\underline{催化劑}}{△}$4NO+6H2O;4NH3+6NO$\frac{\underline{催化劑}}{△}$5N2+6H2O.
點評 本題考查了物質轉化關系的應用和性質應用,主要考查硫及其化合物性質、氮及其化合物、硅及其化合物性質的綜合應用,用好條件是解題關鍵,題目難度中等.


 狀元及第系列答案
狀元及第系列答案 同步奧數系列答案
同步奧數系列答案科目:高中化學 來源: 題型:選擇題
| A. | 電解法、熱分解法、熱還原法 | B. | 熱分解法、電解法、熱還原法 | ||
| C. | 熱還原法、熱分解法、熱還原法 | D. | 電解法、電解法、熱分解法 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
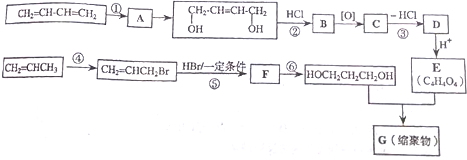
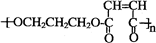 +2nH2O
+2nH2O查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
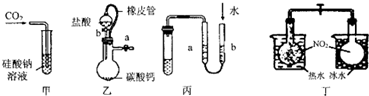
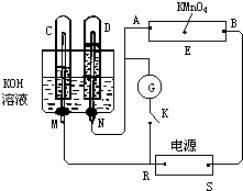
| A. | 甲裝置:可用來證明碳的非金屬性比硅強 | |
| B. | 乙裝置:橡皮管的作用是保證裝置不漏氣 | |
| C. | 丙裝置:用圖示的方法檢查此裝置的氣密性 | |
| D. | 丁裝置:探究溫度對平衡的影響 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.| 選項 | 陳述Ⅰ | 陳述Ⅱ | 判斷 |
| A | 鐵是地殼中含量最高的金屬元素 | 鐵是人類最早使用的金屬材料 | Ⅰ對;Ⅱ對. |
| B | 鋁箔在酒精燈火焰上加熱融化但不滴落 | 鋁箔對熔化的鋁有較強的吸附作用 | Ⅰ對;Ⅱ錯. |
| C | 鋁粉可以和氧化鐵粉末發生鋁熱反應 | 鋁熱反應是工業煉鐵最常用方法 | Ⅰ對;Ⅱ錯. |
| D | 銅在潮濕空氣中表面會生成銅綠 | 可用銅容器盛放濃硫酸 | Ⅰ對;Ⅱ對. |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 制取二氧化氮時,用水或NaOH溶液吸收尾氣 | |
| B. | 用將Fe(NO3)2樣品溶于稀硫酸后,滴加KSCN溶液,觀察溶液是否變紅的方法來檢驗Fe(NO3)2晶體是否變質 | |
| C. | 錐形瓶可用作加熱的反應器 | |
| D. | 只滴加氨水可以鑒別出NaCl、AlCl3、Na2SO4、MgCl2四種溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 工業上常用電解熔融D的氧化物來制備D的單質 | |
| B. | 單質C、D著火,滅火時C不能用泡沫滅火器,但D可以用泡沫滅火器滅火 | |
| C. | 化合物A2B2與C2B2所含化學鍵類型完全相同 | |
| D. | A、B、C組成的化合物,若溶液濃度為0.01mol/L,則由水電離出的OH-為10-12mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
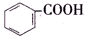 >H2CO3>
>H2CO3>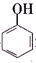 >HCO${\;}_{3}^{-}$,現將
>HCO${\;}_{3}^{-}$,現將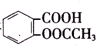 轉變為
轉變為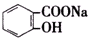 ,可行的方法是( )
,可行的方法是( )| A. | 向該溶液中加入足量的稀硫酸,加熱 | |
| B. | 將該物質與稀硫酸共熱后,再加入足量的NaOH溶液 | |
| C. | 將該物質與稀硫酸共熱后,再加入足量的Na2CO3溶液 | |
| D. | 將該物質與足量的NaOH溶液共熱,再通入足量CO2氣體 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com