
2015年,中國藥學家屠喲坳獲得諾貝爾生理學和醫學獎,其突出貢獻是創制新型抗瘧藥青蒿素和雙氫青蒿素。青蒿素是從黃花篙中提取得到的一種無色針狀晶體,雙氫青蒿素是青蒿素的重要衍生物,抗瘧疾療效優于青蒿素。請回答下列問題:
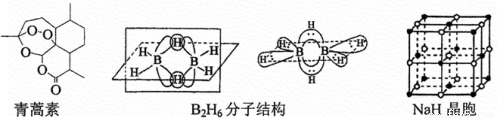
(1)組成青蒿素的三種元素電負性由大到小排序是_________,畫出基態O原子的價電子排布圖_________。(2)一個青蒿素分子中含有_________個手性碳原子;
(3)雙氫青蒿素的合成一般是用硼氫化鈉(NaBH4)還原青蒿素。硼氫化物的合成方法有:
2LiH+B2H6=2LiBH4 4NaH+BF3=NaBH4+3NaF
①寫出BH4-的等電子體_________ (分子、離子各寫一種);
②1976年,美國科學家利普斯康姆(W.N.Lipscomb)因提出多中心鍵的理論解釋B2H6的結構而獲得了諾貝爾化學獎。B2H6分子結構如圖,2個B原子和一個H原子共用2個電子形成3中心二電子鍵,中間的2個氫原子被稱為“橋氫原子”,它們連接了2個B原子。則B2H6分子中有_________種共價鍵,B原子的雜化方式為_________。
③NaBH4的陰離子中一個B原子能形成4個共價鍵,而冰晶石(Na3AlF6)的陰離子中一個Al原子可以形成6個共價鍵,原因是_________。
④NaH的晶胞如圖,則NaH晶體中陽離子的配位數是_________;設晶胞中陰、陽離子為剛性球體且恰好相切,求陰、陽離子的半徑比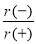 =_________。
=_________。
科目:高中化學 來源:2016屆山西省高三5月月考理綜化學試卷(解析版) 題型:選擇題
電浮選凝聚法是工業上采用的一種污水處理方法,即保持污水的pH在5.0~6.0之間,通過電解生成Fe(OH)3膠體,Fe(OH)3膠體具有吸附作用,可吸附水中的污物而使其沉淀下來,起到凈水的作用,其原理如圖所示。下列說法正確的是
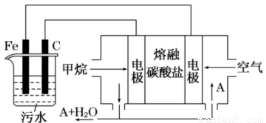
A.石墨電極上發生氧化反應
B.根據圖示,物質A為CO2
C.為增強污水的導電能力,可向污水中加入適量乙醇
D.甲烷燃料電池中CO32—向空氣一極移動
查看答案和解析>>
科目:高中化學 來源:2015-2016學年四川成都七中高一下課后作業乙烯化學試卷(解析版) 題型:選擇題
由乙烯推測丙烯(CH2=CH-CH3)與溴水反應時,下列反應產物正確的是 ( )
A.CH2Br-CH2-CH2Br B.CH3-CBr2-CH3
C.CH3-CH2-CHBr2 D.CH3-CHBr-CH2Br
查看答案和解析>>
科目:高中化學 來源:2015-2016學年貴州省高二下期中理綜化學試卷(解析版) 題型:填空題
[化學—選修2:化學與技術]我國化學侯德榜改革國外的純堿生產工藝,生產流程可簡要表示如下:
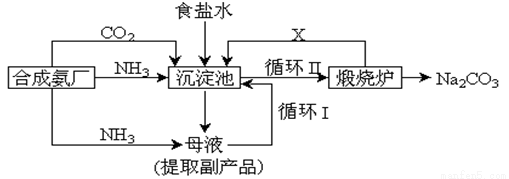
(1)上述生產純堿的方法稱 ,副產品的一種用途為 。
(2)沉淀池中發生的化學反應方程式是 。
(3)寫出上述流程中X物質的分子式 。
(4)使原料氯化鈉的利用率從70%提高到90%以上,主要是設計了 (填上述流程中的編號)的循環。從沉淀池中取出沉淀的操作是 。
(5)為檢驗產品碳酸鈉中是否含有氯化鈉,可取少量試樣溶于水后,再滴加 。
(6)向母液中通氨氣,加入細小食鹽顆粒,冷卻析出副產品,通氨氣的作用有 。
A.增大NH4+的濃度,使NH4Cl更多地析出
B.使NaHCO3更多地析出
C.使NaHCO3轉化為Na2CO3,提高析出的NH4Cl純度
查看答案和解析>>
科目:高中化學 來源:2015-2016學年貴州省高二下期中理綜化學試卷(解析版) 題型:選擇題
煤是“工業的糧食”,石油是“工業的血液”。有關煤和石油加工的說法正確的是
A.煤的干餾產物主要是各類有機物
B.石油的裂解、分餾和煤的干餾都屬于化學變化
C.煤焦油經過分餾可得到苯、甲苯等,說明煤中含有苯和甲苯
D石油的裂化,說明長鏈烴在高溫條件下可以分解為短鏈烴
查看答案和解析>>
科目:高中化學 來源:2015-2016學年黑龍江省高一下期中化學試卷(解析版) 題型:填空題
現有部分短周期元素的性質或原子結構如下表:
元素編號 | 元素性質或原子結構 |
X | 最外層電子數是次外層電子數的2倍 |
Y | 常溫下單質為雙原子分子,其氫化物水溶液呈堿性 |
T | 最外層電子數是電子層數的3倍 |
Z | 元素最高正價是+7價 |
(1)元素X的一種同位素可測定文物年代,這種同位素的符號是__________;X的一種氫化物燃燒時火焰溫度高,可以焊接金屬,則該氫化物的結構式為 ;實驗室制取該氣體的化學方程式是 。
(2)將9g單質X在足量氧氣中燃燒,所得氣體通入1L 1mol·L-1 NaOH溶液中,完全吸收后,將溶液在減壓低溫條件下蒸干,得到不含結晶水的固體質量為 g。
(3)元素Y與氫元素形成一種離子YH,寫出該微粒的電子式____________(用元素符號表示)。實驗室檢驗該微粒的方法是: 。
(4)T元素在周期表的位置: ,其簡單陰離子的結構示意圖: , 證明該粒子的還原性比Z— 強的離子方程式是 。硒(Se)是人體必需的微量元素,與T在同一主族,Se原子比T原子多一個電子層,則Se的原子序數為________,其最高價氧化物對應的水化物的化學式為________。
(5)元素Z與氫氧化鈉溶液反應的化學方程式為 ,其生成的含氧酸鹽的電子式為 。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年黑龍江省高一下期中化學試卷(解析版) 題型:選擇題
下列關于元素性質的有關敘述中正確的是
A.可以用HClO和H2SO3酸性的相對強弱來比較Cl和S的非金屬性強弱
B.金屬和非金屬之間一定能形成離子化合物
C.堿金屬元素單質,由Li→Fr,熔點逐漸降低
D.沸點:HI>HBr>HCl>HF
查看答案和解析>>
科目:高中化學 來源:2015-2016學年黑龍江大慶市高一下期中化學試卷(解析版) 題型:填空題
現有反應mA(g)+nB(g) pC(g),達到平衡后,當升高溫度時,B的轉化率減小;當減小壓強時,混合體系中A的質量分數增大,則
pC(g),達到平衡后,當升高溫度時,B的轉化率減小;當減小壓強時,混合體系中A的質量分數增大,則
(1)該反應的正反應是__________熱反應,且m+n__________p (填“>”、“<”或“=”)。
(2)增大壓強時,B的轉化率__________(填“增大”、“減小”或“不變”,下同),逆反應速率__________。
(3)若加入C(體積不變),則A的體積分數__________。
(4)若降低溫度,則平衡時B、C的濃度之比c(C)/c(B)比值將________。
(5)若加入催化劑,該反應的反應熱________。
(6)若B是有色物質,A、C均為無色物質,維持容器體積不變,充入氖氣時,混合氣體的顏色__________(填“變淺”、“變深”或“不變”)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com