
分析 (1)等物質的量的以上物質燃燒時,分子中C、H原子數目越大,生成CO2、水越多;烴(CxHy)的物質的量相等,完全燃燒耗氧量取決于(x+$\frac{y}{4}$)值,該值越大,耗氧量越多消耗的氧氣越多;
(2)等質量的烴完全燃燒,C的質量分數越大,生成的二氧化碳越多,H元素質量分數越大,生成的水越多,耗氧量越大.
解答 解:(1)等物質的量的以上物質燃燒時,分子中C、H原子數目越大,生成CO2、水越多,則生成CO2最多的是丙烷,生成的水最多的是丙烷;烴(CxHy)的物質的量相等,完全燃燒耗氧量取決于(x+$\frac{y}{4}$)值,該值越大,耗氧量越多消耗的氧氣越多,則耗氧量最大的是丙烷;由此可以得出結論:等物質的量的烷烴完全燃燒,生成CO2、H2O以及消耗O2的量隨著 分子中碳原子數的增多而變大
故答案為:丙烷;丙烷;丙烷;分子中碳原子數;
(2)等質量的烴完全燃燒,C的質量分數越大,生成的二氧化碳越多,丙烷中碳的質量分數為$\frac{36}{36+8}$,乙烷中碳的質量分數為$\frac{24}{24+6}$,甲烷中碳的質量分數為$\frac{12}{12+4}$,則丙烷的碳的質量分數最大,生成的二氧化碳最多;H元素質量分數越大,生成的水越多,耗氧量越大,甲烷中碳的質量分數最小,則氫的質量分數最大,所以甲烷消耗的氧氣最多,生成的水最多;由此可以得出結論:等質量的烷烴完全燃燒,生成CO2的量隨著 分子中碳的質量分數的增大而變大,生成水的量隨著 分子中氫的質量分數的增大而變大,消耗O2的量隨著 分子中氫的質量分數的增大而變大,
故答案為:丙烷;甲烷;甲烷;分子中碳的質量分數;分子中氫的質量分數;分子中氫的質量分數.
點評 本題考查有機物燃燒有關計算,難度不大,注意根據燃燒通式及元素質量分數理解烴耗氧量.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 化學鍵是一種作用力 | |
| B. | 化學鍵可以使離子相結合,也可以使原子相結合 | |
| C. | 非極性鍵不是化學鍵 | |
| D. | 化學反應過程中,反應物分子內的化學鍵斷裂,產物分子中的化學鍵形成 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 溴乙烷中滴入AgNO3溶液檢驗其中的溴元素:Br-+Ag+=AgBr↓ | |
| B. | 用醋酸除水垢:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| C. | 利用腐蝕法制作印刷線路板:Fe3++Cu=Fe2++Cu2+ | |
| D. | 實驗室用溴和苯在催化劑作用下制溴苯: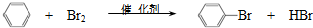 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cl2與水的反應:Cl2+H2O═2H++Cl-+ClO- | |
| B. | H2SO4與Ba(OH)2反應:Ba2++SO42-═BaSO4 | |
| C. | 足量鐵溶于稀硝酸:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| D. | AlCl3溶液中加入過量稀氨水:Al3++3NH3•H2O═Al(OH)3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將pH=5的醋酸溶液稀釋后,恢復至原溫度,pH和Kw均增大 | |
| B. | 25℃時,pH=3的氯化銨溶液中:c(OH-)=1.0×10-11mol•L-1 | |
| C. | 25℃時,pH=4的氯化銨溶液中:c(Cl-)>c(NH4+)>c(H+)>c(OH-) | |
| D. | 向NH4HSO4溶液中加入等物質的量的NaOH形成的溶液中:c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙烷不能使酸性高錳酸鉀褪色,故苯乙烷也不能使酸性高錳酸鉀褪色 | |
| B. | 乙醛與乙酸都含有碳氧雙鍵,故都能與H2發生加成反應 | |
| C. | 甲酸鈉結構中含有醛基,能發生銀鏡反應,故甲酸甲酯也能發生銀鏡反應 | |
| D. | 甲烷與氯氣在光照下反應可生成一氯甲烷,甲苯與氯氣在光照下反應主要生成2,4-二氯甲苯 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 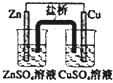 如裝置中,鹽橋中的K+移向CuSO4溶液 | |
| B. | 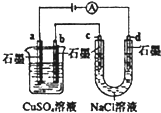 如圖裝置中b極析出6.4g固體時,d極產生2.24LH2 | |
| C. | 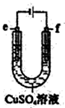 用如圖裝置精煉銅時,f極為粗銅 | |
| D. | 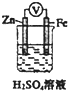 如圖裝置中電子沿導線由Zn流向Fe,Fe極上有大量氣泡生成 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com