
等物質的量的鈉、鎂、鋁分別與1L1mol/L的鹽酸作用產生氫氣,可出現下列四種情況:①Na<Mg<Al;②Na<Mg=Al;③Na=Mg=Al;④Na>Mg=Al.討討論上述四種情況所需金屬的物質的量分別在何范圍?
①n<1/2 ② 1/2≤n<1
![]() ③n=1 ④n>1
③n=1 ④n>1
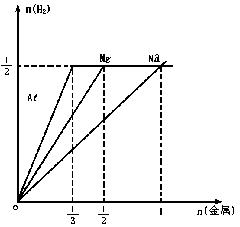
化學反應中,反應物與生成物的量通常成線性關系,作圖時可利用特殊點(如剛開始反應,恰好完全反應等)畫出投入金屬量與產生氫氣量的關系圖,各種情況一目了然.
![]()
![]() 根據Na~H+~ H2 Mg~2H+~H2
根據Na~H+~ H2 Mg~2H+~H2
![]() Al~3H+~ H2
Al~3H+~ H2
![]() 對于Na:起點O(0,0),鹽酸恰好完全反應時為A點(1,1/2 );
對于Na:起點O(0,0),鹽酸恰好完全反應時為A點(1,1/2 );
![]() 對于Mg:起點O(0,0),鹽酸恰好完全反應時為B點( 1/2、1/2 );
對于Mg:起點O(0,0),鹽酸恰好完全反應時為B點( 1/2、1/2 );
![]() 對于Al:起點O(0,0),鹽酸恰好完全反應時為C點(1/3 ,1/2 )
對于Al:起點O(0,0),鹽酸恰好完全反應時為C點(1/3 ,1/2 )
![]() 顯然,當n<1/2 時,Na<Mg<Al
顯然,當n<1/2 時,Na<Mg<Al
![]() 當 1/2≤n<1時,Na<Mg=Al
當 1/2≤n<1時,Na<Mg=Al
![]() 當n=1時,Na=Mg=Al
當n=1時,Na=Mg=Al
![]() 當n>1時,Na>Mg=Al.
當n>1時,Na>Mg=Al.


 初中學業考試導與練系列答案
初中學業考試導與練系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
(2)等質量的鈉、鎂、鋁與足量的鹽酸反應,在相同條件下產生氫氣的體積之比是__________。
(3)若產生相同體積(同溫同壓下)的氫氣,所需鈉、鎂、鋁的物質的量之比是__________。
(4)若產生相同體積(同溫同壓下)的氫氣,所需鈉、鎂、鋁的質量之比是_______________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com